 全部药品分类
全部药品分类
 全部药品分类
全部药品分类
 1389
1389
阿帕替尼简要说明书:
药品中文名:甲磺酸阿帕替尼片
药品英文名:Apatinib
药品中文商品名: 艾坦
小分子多靶点TKI:靶向VEGFR1、VEGFR2、VEGFR3、PDGFR-β、C-KIT、FGFR1和FLT3
生产厂家:江苏恒瑞医药股份有限公司
中国上市:2014年获批上市
规格剂量价格:425mg*14粒,4620元/盒;250mg*10粒,2226元/盒。
医保报销:医保乙类,可报销,医保报销后大概600-1300元
医保适应症/医保报销条件:
1.本品单药用于既往至少接受过2种系统化疗后进展或复发的晚期胃腺癌或胃-食管结合部腺癌患者。患者接受治疗时应一般状况良好。
2.本品单药用于既往接受过至少一线系统性治疗后失败或不可耐受的晚期肝细胞癌患者。
适应症及用途:
1. 本品单药用于既往至少接受过2种系统化疗后进展或复发的晚期胃腺癌或胃-食管结合部腺癌患者。患者接受治疗时应一般状况良好。
2. 本品单药用于既往接受过至少一线系统性治疗后失败或不可耐受的晚期肝细胞癌患者。
3. 本品联合注射用卡瑞利珠单抗用于不可切除或转移性肝细胞癌患者的一线治疗。
用法用量:
推荐剂量:850mg或者750mg或者500mg(体力状态评分ECOG≥2、四线化疗以后、胃部原发癌灶没有切除、骨髓功能储备差以及年老体弱或瘦小的女性患者,可以先从500 mg qd开始服药,1~2 周后再酌情调整剂量),每日1次。
服用方法:口服,餐后半小时服用(每日服药的时间应尽可能相同),以温开水送服。
剂量调整:在本品使用过程中应密切监测不良反应,并根据需要进行调整以使患者能够耐受治疗。阿帕替尼所致的不良反应可通过对症治疗、停药和调整剂量等方式处理。临床研究中剂量调整多发生在第2、3个周期(28天为一周期)。
不良反应:
主要副作用有高血压、蛋白尿、手足综合征、腹泻,此外还包括乏力、口腔溃疡和声音嘶哑等。
作用机制:
艾坦/阿帕替尼是通过高度选择性竞争细胞内VEGFR-2的ATP结合位点,抑制酪氨酸激酶的生成从而抑制肿瘤组织新血管的生成,阻断下游信号传导,从而强效抗肿瘤组织血管生成,最终达到全方位打击肿瘤的目的。
肝癌治疗由靶向时代进入免疫时代:
近几年来,肿瘤免疫治疗被认为是癌症治疗领域最成功的方法之一,在《科学》杂志2013年十大科学突破中位居首位。与传统肝癌治疗手段相比,免疫治疗发生严重毒性反应的概率更低,患者耐受性更好,可有效增强机体的免疫反应,延缓肿瘤的进展1。因此,免疫疗法已成为当下晚期肝癌系统治疗的主要治疗方式。
尽管免疫治疗在晚期肝癌治疗中取得重大进展,治疗后中位OS为8.2~17个月2,但研究结果表明免疫单药方案治疗应答仍然较低3。而免疫检查点抑制剂和抗血管靶向药物联合治疗(靶免联合)可让大多数患者获得持久的缓解,提高临床获益,或引起肝癌治疗模式的转变4。
那么在免疫时代下,应该如何选择靶向药物才能起到“1+1>2”的作用?
药物研发,机制先行。本文将从疾病与治疗机制出发,探讨与免疫检查点抑制剂联用的靶向药物需满足的机制特点。
从机制出发看免疫时代下靶向药物的选择:
免疫治疗的机制与T细胞有密切关联。免疫检查点是在一系列免疫反应中传递共刺激或共抑制信号的分子,主要包括程序性死亡受体1(PD-1)/程序性死亡受体-配体1(PD-L1)、程序性死亡受体-配体2(PD-L2)等。其中PD-1表达在活化的T淋巴细胞表面,通过与其配体PD -L1和PD -L2结合,抑制抗原特异性T淋巴细胞活化5。针对这一机制,免疫检查点抑制剂(抗PD-1或抗PD-L1)通过阻断受体与配体的结合,促进T淋巴细胞对肿瘤细胞的杀伤作用5。
为了充分发挥免疫治疗的优势,起到“1+1>2”的作用,在肿瘤免疫治疗时代下,靶向药物的选择需要考虑对免疫治疗有无正负向的影响。
从机制角度来看,抗血管生成靶向治疗与血管内皮生长因子(VEGF)、细胞毒性T淋巴细胞相关蛋白4(CTLA4)、表皮生长因子受体(EGFR)等一系列靶点有关。其中VEGF家族蛋白表达后与受体相互结合发挥功能,而酪氨酸激酶受体(VEGFRs)分为VEGFR-1、VEGFR-2和VEGFR-36,其中VEGFR-2在血管发生和血管生成中起首要作用,VEGFR-3则主要与淋巴管的生成相关7。
针对肿瘤血管异常导致肿瘤微环境发生缺氧和酸中毒,进而通过多种机制造成免疫抑制,而VEGFR-2抗血管生成治疗可通过使肿瘤周围血管正常化,改善肿瘤微环境8,进而促进免疫治疗的效果。
而淋巴管在免疫反应中扮演关键角色,促进T细胞活化与浸润。VEGFR-3主要在淋巴管内皮细胞中表达,刺激内皮细胞增殖,从而在淋巴管生成中起关键作用9。
因此,抗血管生成靶向治疗如果抑制了VEGFR-3靶点,对肿瘤免疫治疗是产生负向抑制作用。此时联合免疫治疗,将不会起到1+1>2,甚至只会1+1=1。
小分子TKI可能是免疫时代下靶向药物的更佳选择,但选择怎样的小分子药物需要更加全面的考虑
目前已公布研究结果的3个小分子TKI(酪氨酸激酶抑制剂)靶免联合方案用于晚期肝癌一线治疗的Ⅲ期临床研究中,仅有1个获得成功,即阿帕替尼。
小分子靶向药物联合免疫用于晚期肝癌一线治疗的Ⅲ期临床研究与结果
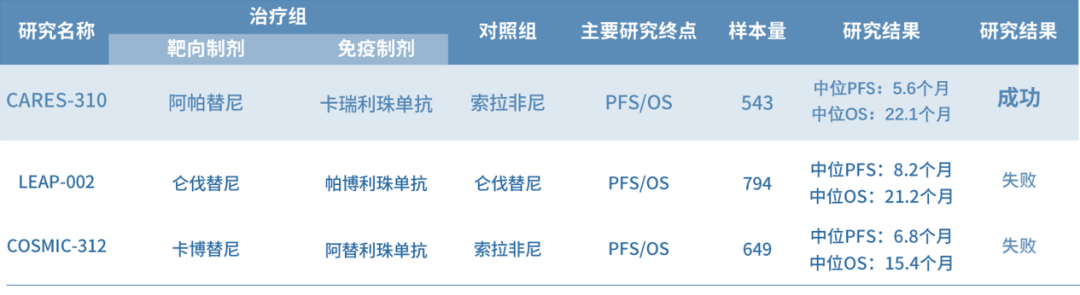
免疫疗法已成为当下肿瘤学的主要治疗方式,在肿瘤免疫治疗时代下,靶向药物的选择需避免对免疫治疗的负向作用。VEGFR-3受体通路刺激淋巴管的生成,从而间接促进T细胞运输至肿瘤细胞,促进T细胞在肿瘤部位的活化与浸润。因此,抑制VEGFR-3靶点对肿瘤免疫治疗是负向抑制作用。而阿帕替尼不抑制VEGFR-3,高度选择性抑制VEGFR-2,具有抗血管生成、改善肿瘤乏氧环境、不破坏淋巴-免疫体系三重抗肿瘤机制。由于对免疫治疗无负向作用,阿帕替尼联合卡瑞利珠单抗的靶免方案一线治疗晚期肝癌安全有效,开启了治疗新格局。
目前有多家机构正在开展阿帕替尼用于治疗这类患者的临床试验,以期能够尽快改善治疗效果。由此可见相应治疗效果将会具有更良好的前景。