Mobocertinib莫博替尼/安卫力
莫博赛替尼是目前中国首个且唯一获批针对 EGFR ex20ins 突变 NSCLC 的口服 TKI,并且被纳入美国国立综合癌症网络(NCCN)指南和中国临床肿瘤学会(CSCO)指南推荐。
在一项全球 I 期、II 期以及 EXCLAIM 延展队列研究中,莫博替尼表现出如下特点优势:
1、缓解时间持久:
独立评审委员会(IRC)评估的 ORR 为 28%, 研究者(INV)评估的 ORR 为 35%,中位缓解持续时间(DoR)长达 15.8 个月;莫博赛替尼治疗后疾病控制率(DCR)高达 78%,84% 患者实现缩瘤。
2、生存时间延长:
莫博赛替尼改善铂类经治患者的生存获益,中位 PFS 达 7.3 个月,中位 OS 长达 20.2 个月。
莫博赛替尼简要说明书:
药品中文名:琥珀酸莫博赛替尼胶囊
药品中文商品名:安卫力
药品英文名:Mobocertinib
药品英文商品名:Exkivity
药品别名:莫博替尼、莫博赛替尼
研发代号:TAK-788
基因靶点:EGFR ex20ins
包装规格:40mg*112粒/盒,14粒/板,8板/盒
生产厂家:日本武田制药
中国上市:2023年1月11日在中国获批上市
中国上市价格:37588元/28天
医保报销:无医保报销
适应症及用途:
EXKIVITY是一种激酶抑制剂,适用于治疗具有表皮生长因子受体(EGFR)外显子20插入突变的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者,经FDA批准的测试检测到,其疾病在铂类化疗期间或之后进展。根据总体反应率和反应持续时间,该适应症在加速批准下获得批准。对该适应症的持续批准可能取决于验证性试验中对临床益处的验证和描述。
不良反应及处理方法
最常见(>20%)的不良反应是腹泻、皮疹、恶心、口腔炎、呕吐、食欲下降、甲沟炎、疲劳、皮肤干燥和肌肉骨骼疼痛。
最常见的(≥2%)3或4级实验室异常是淋巴细胞减少,淋巴细胞增加淀粉酶、脂肪酶增加、钾减少、血红蛋白减少、肌酐增加和镁减少。
用法用量:
成人推荐剂量:除医嘱外,160mg每天一次口服,空腹或餐后2小时服用。
作用机制:
Mobocertinib是一种表皮生长因子受体(EGFR)激酶抑制剂,在低于野生型(WT)EGFR的浓度下不可逆地结合并抑制EGFR外显子20插入突变。两种药理活性代谢物(AP32960和AP32914)与mobocertinib具有相似的抑制特性 已在口服莫博替尼后的血浆中发现。
在体外,mobocertinib还在临床相关浓度(IC50值<2nM)下抑制其他EGFR家族成员(HER2和HER4)和一种额外激酶(BLK)的活性。
在培养的细胞模型中,mobocertinib以比WT-EGFR信号传导抑制低1.5至10倍的浓度抑制由不同EGFR外显子20插入突变变体驱动的细胞增殖。
药物相互作用:
CYP3A抑制剂:避免EXKIVITY与强或中度CYP3A抑制剂同时使用。如果不可避免地同时使用中度 CYP3A抑制剂,则减少EXKIVITY的剂量。
CYP3A 诱导剂:避免EXKIVITY与强或中度CYP3A诱导剂同时使用。
在特定人群中使用:
哺乳期:建议不要母乳喂养。
注意事项:
•EXKIVITY可导致危及生命的心率校正QT(QTc)延长,包括尖端扭转型室性心动过速,这可能是致命的,需要监测QTc和在基线和治疗期间定期检查电解质。
增加有QTc延长危险因素的患者的监测频率。
•避免使用已知会延长QTc间期的伴随药物,以及使用强或中度CYP3A抑制剂与EXKIVITY,这可能会进一步延长QTc。
•根据QTc延长的严重程度不给、减少剂量或永久终止EXKIVITY。
间质性肺病(ILD)/肺炎:监测患者是否出现新的或恶化的表明ILD/肺炎的肺部症状。对疑似ILD/肺炎患者立即停用EXKIVITY,如果确认ILD/肺炎,则永久终止EXKIVITY。
心脏毒性:在基线和治疗期间监测心脏功能,包括左心室射血分数。扣留、减低剂量恢复或根据严重程度永久停药。
腹泻:腹泻可能导致脱水或电解质失衡,无论有无肾功能损害。监测电解质并建议患者在腹泻第一次发作时开始使用止泻药并增加液体和电解质的摄入量。根据严重程度扣留、减少剂量或永久终止 EXKIVITY。
胚胎-胎儿毒性:可能对胎儿造成伤害。忠告有生育潜力的女性对胎儿的潜在风险并使用有效的非激素避孕药。
临床数据:
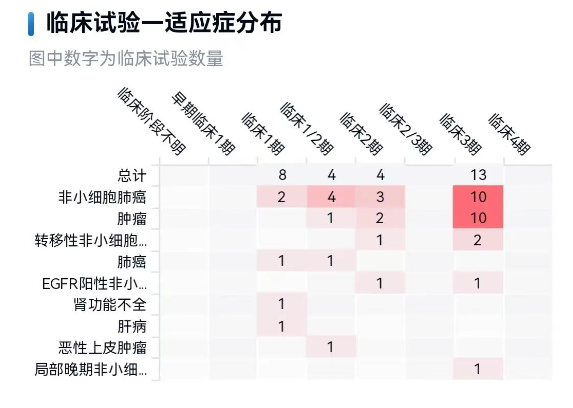
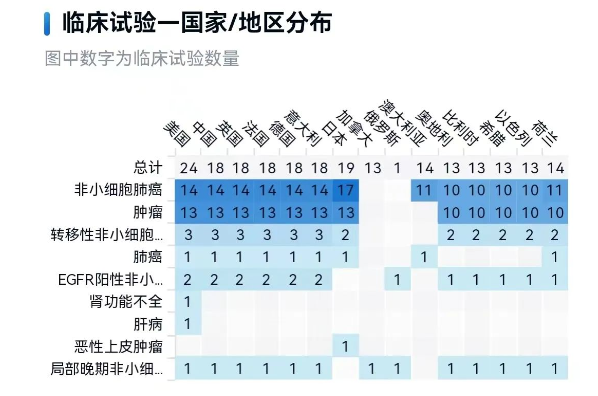
NCT02716116是一项开放标签试验,试验共入组137名NSCLC患者,其中EGFR外显子20插入突变的患者28名。55名患者每日接受一次TAK-788,每次5~180mg(剂量递增试验);剩余72名患者(包括28名EGFR外显子20插入突变患者)每日接受一次TAK-788,每次160mg。
所有患者的人群特征为:中位年龄61岁,71%为女性。75%为白人,14%为亚洲人,6%为黑人,5%为其他种族。94%的患者为腺癌。26%的患者ECOG评分为0,73%的患者ECOG评分为1。
患者的中位治疗方案为3。4%的患者先前未接受过治疗,23%的患者先前接受过1种治疗方案,25%的患者先前接受过2种治疗方案,48%的患者接受过3种或以上的治疗方案。31%的患者先前接受过EGFR/HER2 TKI治疗,44%的患者先前接受过检查点抑制剂治疗。
71%的患者从不吸烟,29%的患者以前吸烟。47%的患者在基线时有脑转移。
试验结果表明, EGFR外显子20插入突变患者的ORR为43%,PR为43%,SD为43%。疾病控制率为86%,中位PFS为7.3个月。
在EGFR外显子20插入突变的患者中,12名患者在基线时有脑转移,16名患者无脑转移。两组患者(有脑转移 VS 无脑转移)的ORR为25% VS 56%,PR为25% VS 56%,SD为42% VS 44%,疾病控制率为67% VS 100%,中位PFS为3.7个月 VS 8.1个月。
不良反应
所有患者中,最常见的不良反应有:腹泻(74%)、恶心(33%)、皮疹(26%)、呕吐(22%)、食欲下降(22%)、口腔炎(14%)、脂肪酶增加(8%)、淀粉酶增加(8%)。
所有患者中,最常见的3级以上不良反应有:腹泻(12%)、恶心(4%)、口腔炎(3%)、脂肪酶增加(3%)、淀粉酶增加(3%)、呕吐(2%)、皮疹(1%)、食欲下降(1%)。
接受160mg剂量的患者中,最常见的不良反应有:腹泻(85%)、恶心(43%)、皮疹(36%)、呕吐(29%)、食欲下降(25%)、口腔炎(18%)、脂肪酶增加(10%)、淀粉酶增加(8%)。
接受160mg剂量的患者中,最常见的3级以上不良反应有:腹泻(18%)、恶心(6%)、脂肪酶增加(6%)、口腔炎(4%)、淀粉酶增加(4%)、呕吐(3%)、皮疹(1%)、食欲下降(1%)。
TAK-788(每日一次,每次160mg)对EGFR外显子20插入突变的患者具有抗肿瘤活性,患者的ORR为43%,中位PFS为7.3个月;
TAK-788的不良反应与其他EGFR TKIs一致,且是可控的。