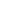2023年2月17日,FDA批准使用斯帕生坦减少有疾病快速进展风险的原发性免疫球蛋白A肾病(IgAN)成人的蛋白尿,并基于减少蛋白尿加速批准。斯帕生坦最初是为治疗高血压而开发的;然而,它已被证明可有效减少 IgAN 和局灶节段性肾小球硬化症(FSGS)患者的蛋白尿。与厄贝沙坦相比,斯帕生坦在更大程度上减少了蛋白尿。此外,它是第一个减少IgAN蛋白尿的非免疫抑制疗法。
斯帕生坦是内皮素A型受体(ET一个R)和血管紧张素II(Ang II)1型受体(AT1R)对两者具有相似的亲和力(ET为9.3 nM一个R 和 0.8 nM 用于 AT1R).斯帕生坦是同类产品中的第一个,具有口服活性,是通过合并厄贝沙坦的结构元素而制成的。
患者吃斯帕生坦治疗需要吃多久?
斯帕生坦的治疗持续时间可能在3-6个月,甚至更久。
斯帕生坦的初始剂量为200mg,14天后可根据患者对药物的耐受情况增加到400mg,具体治疗持续时间应根据患者的情况判断。如果患者病情较轻,可能用药3个月左右病情得到控制、好转,但如果患者疾病严重通常需要服用更长的时间,如6个月左右,甚至更长,具体应在医生的评估下明确。
斯帕生坦的临床疗效结果如何?
背景:局灶节段性肾小球硬化(FSGS)治疗的需求尚未得到满足。在一项为期8周的2期试验中,一种双重内皮素-血管紧张素受体拮抗剂sparsentan减少了FSGS患者的蛋白尿。长期使用斯帕生坦治疗FSGS的疗效和安全性尚不清楚。
方法:在这个3期试验中,招募了8-75岁的FSGS患者(没有已知的次要原因),患者被随机分配接受斯帕生坦或irbesartan(活性对照)治疗108周。在36周时预先指定的中期分析中评估的替代疗效终点是蛋白尿的FSGS部分缓解终点(定义为尿蛋白与肌酐的比率≤1.5[蛋白和肌酐均以克计],且该比率比基线下降>40%)。主要疗效终点是最终分析时估计的肾小球滤过率(eGFR)斜率。从基线到治疗结束后4周(第112周)eGFR的变化是次要终点。
结果:共有371例患者接受了随机分组:184例被分配接受斯帕森坦治疗,187例接受厄贝沙坦治疗。在第36周,蛋白尿部分缓解的患者百分比在斯帕生坦组为42.0%,在irbesartan组为26.0%,这一反应持续了108周。在第108周的最终分析时,eGFR斜率没有显著的组间差异;总斜率的组间差异(第1天至第108周)为每年每1.73平方米体表面积每分钟0.3毫升(95%置信区间[CI],-1.7至2.4),从第6周至第108周的斜率(即慢性斜率)的组间差异为每年每1.73平方米每分钟0.9毫升(95%CI,-1.3至3.0)。从基线到第112周的eGFR的平均变化是:使用斯帕生坦的每1.73m2每分钟-10.4ml,使用irbesartan的每1.73m2每分钟-12.1ml(差异,每1.73m2每分钟1.8ml;95%可信区间为-1.4至4.9)。斯帕生坦和irbesartan具有相似的安全性,两组的不良事件发生率相似。
结论:在FSGS患者中,108周时eGFR斜率没有显著的组间差异,尽管与厄贝沙坦相比,使用斯帕生坦可以更大程度地减少蛋白尿。

斯帕生坦简要说明书
通用名称:sparsentan
商品名称:Filspari
全部名称:sparsentan、Filspari、斯帕生坦、司帕生坦
适应症:
FILSPARI 适用于减少有快速疾病进展风险的原发性免疫球蛋白 A 肾病 (IgAN) 成人患者的蛋白尿,通常为尿液蛋白肌酐比 (UPCR)≥1.5 g/g.
用法用量:
1、一般注意事项
开始 FILSPARI 治疗前,停止使用肾素-血管紧张素-醛固酮系统 (RAAS) 抑制剂、内皮素受体拮抗剂 (ERA) 和阿利吉仑 [见禁忌症]。
2、监测
1)仅在测量转氨酶水平和总胆红素后,开始 FILSPARI 治疗胆红素。转氨酶升高 (> 3x ULN) 的患者应避免启动治疗。在开始治疗后的前12个月内,需要继续每月监测一次,或在因转氨酶升高而中断治疗后重新开始监测,然后在 FILSPARI 治疗期间每3个月监测一次 [参见用法用量、警告和注意事项]。
2)只有在确认妊娠试验阴性后才能妊娠的患者开始 FILSPARI 治疗。在 FILSPARI 治疗期间和停止治疗后1个月,要求每月进行一次妊娠试验 [参见警告和注意事项、特殊人群用药]。
3、推荐剂量
开始 FILSPARI 治疗,200 mg口服,每日一次。14天后,根据耐受情况增加至推荐剂量 400 mg 每日一次。中断后重新开始 FILSPARI 治疗时,应考虑从 200 mg 每日一次开始滴定FILSPARI.14天后,增加至推荐剂量 400 mg 每日一次。
4、给药
指导患者在早餐或晚餐前用水整片吞服片剂。保持与进餐相同的给药模式。如果漏服一剂药物,在定期计划时间服用下一剂药物。请勿服用双倍剂量或额外剂量。
5、针对转氨酶升高的剂量调整
如果转氨酶水平升高,根据表1调整监测和治疗计划。
对于出现肝毒性临床症状的患者或肝酶水平和胆红素未恢复至治疗前水平的患者,请勿重新开始治疗。
6、与强效 CYP3A 抑制剂合并使用时的剂量调整
避免强效 CYP3A 抑制剂与 FILSPARI 合并使用。
如果无法避免强效 CYP3A 抑制剂,则中断 FILSPARI 治疗。
不良反应:
1、外周水肿
患者可能出现外周水肿的情况,身体的四肢、手指、脚踝等部位出现水液潴留所致的肿胀。
2、低血压
使用司帕生坦的患者可能会出现低血压的情况,包括体位性低血压。体位性低血压指的是从坐位或躺位突然站立时,出现血压下降和晕厥的现象。患者在使用司帕生坦期间应注意体位变换时的缓慢起立,以避免低血压引起的不适。
3、头晕
患者也可能会感到头晕、眩晕或晕眩的感觉。头晕可能由于血压下降、血流改变或其他因素引起。
4、高钾血症
使用司帕生坦的患者可能会出现高钾血症的情况,患者血液中的钾离子浓度升高,可能对心脏功能产生影响。如果患者出现高钾血症症状,如心律不齐、肌肉无力等,应及时告知医生,并进行相关的检查和治疗。
5、贫血
患者也可能有贫血的情况,血液中的红细胞数量或血红蛋白浓度降低,可能导致乏力、疲倦等症状。
注意事项:
1、您的医生在定期就诊时检查您的进展非常重要。可能需要进行血液和尿液检查以检查不良反应。您的医生将在开始治疗前进行检查,每月进行一次检查,持续 12 个月,然后在使用该药物治疗期间每 3 个月进行一次检查。
2、不要将这种药物与阿利吉仑(Tekturna®)或其他血压药物(例如血管紧张素受体阻滞剂,内皮素受体阻滞剂)一起使用。
3、怀孕期间使用这种药物会伤害您未出生的婴儿。如果您是可以怀孕的女性,您的医生将在开始前、治疗期间和停用此药后 1 个月内进行检查,以确保您没有怀孕。在开始前、治疗期间以及最后一次服药后 1 个月内使用有效的避孕形式,以防止怀孕。询问您的医生哪种形式的节育措施适合您。如果您认为自己在使用药物时怀孕了,请立即告诉您的医生。
4、这种药物可能会导致严重的肝脏问题。如果您有尿色深、疲劳、食欲不振、恶心或呕吐、严重胃痛或眼睛或皮肤发黄,请立即咨询您的医生。
5、如果您突然从躺着或坐着的姿势站起来时出现视力模糊、意识模糊、头晕、昏厥或头晕、出汗或异常疲倦或虚弱,请立即咨询您的医生。这些可能是低血压(低血压)的症状。
6、这种药物可能会导致严重的肾脏问题。如果您有躁动、昏迷、意识模糊、尿量减少、抑郁、头晕、头痛、敌意、易怒、嗜睡、肌肉抽搐、恶心、体重快速增加、癫痫发作、木僵、面部、脚踝或手肿胀或异常疲倦或虚弱,请立即咨询您的医生。
7、如果您有意识模糊、心律不齐、恶心或呕吐、紧张、手、脚或嘴唇麻木或刺痛、胃痛、呼吸困难或腿部无力或沉重,请立即咨询您的医生。这些可能是高钾血症(血液中钾含量高)的症状。
8、这种药物可能会导致体液潴留(体内水分过多)。如果您有尿量减少、嘈杂、嘎嘎作响或呼吸困难、面部、手、脚或小腿肿胀或体重增加,请立即咨询您的医生。
9、除非已与您的医生讨论过,否则不要服用其他药物。这包括处方药或非处方药(非处方药 [OTC])以及草药或维生素补充剂。
禁忌症:
妊娠患者禁用 FILSPARI.
FILSPARI 不得与血管紧张素受体阻滞剂 (ARB)、ERA或阿利吉仑。
贮存方法:
储存于20°C-25°C(68°F-77°F),允许波动范围为15°C-30°C(59°F-86°F)。
将 FILSPARI 储存在其原始容器中。