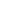艾伏尼布成为了首款获批用于治疗IDH1突变MDS的靶向药物。这也是艾伏尼布在美国获批的第4项适应症。2023年10月24日,FDA官网显示:施维雅(Servier)的艾伏尼布片(ivosidenib,商品名:Tibsovo)获批用于治疗IDH1突变的复发性或难治性骨髓增生异常综合征(R/R MDS)。
FDA此次批准主要是基于一项开放标签、剂量递增、剂量扩展I期研究(AG120-C-001)的积极结果。该研究共纳入18例携带IDH1突变的R/R MDS患者,评估了艾伏尼布(500mg,每日1次)在这类患者中的安全性、有效性、药代动力学(PK)、药效学(PD)性质。
结果显示,实现完全缓解(CR)的患者比例为38.9%,实现客观缓解的患者比例为83.3%,中位总生存期(OS)为35.7个月。在9例依赖输血的患者中,有6例在接受艾伏尼布治疗后至少56天内不需要输血。艾伏尼布的安全性与既往研究一致。
艾伏尼布是Agios Pharmaceuticals开发的一款针对IDH1突变的小分子抑制剂,后来其权益归施维雅和基石药业所有。基石药业拥有艾伏尼布的中国权益,施维雅则拥有该产品在中国以外的所有权益。据估计,美国每年有16000例MDS患者确诊。大约3.6%的MDS患者携带IDH1突变,这类突变被认为是MDS的早期驱动因素。携带IDH1突变的MDS患者通常预后不良并且在后期进展为急性髓系白血病(AML)的风险也增加。
在美国,艾伏尼布被批准用于治疗患有 IDH1 突变的复发或难治性 AML 的成人患者,以及单药治疗或与阿扎胞苷联合治疗年龄≥75 岁或患有妨碍治疗的合并症的新诊断 IDH1 突变 AML 的成人患者。使用强化诱导化疗作为单一疗法治疗 IDH1 突变复发或难治性 MDS 成年患者;以及既往接受过 IDH1 突变胆管癌治疗的患者。
艾伏尼布 是一种精准药物,针对一种称为异柠檬酸脱氢酶 1 (IDH1) 的特定类型突变。艾伏尼布在全球获得了五种适应症的批准,包括在美国、欧盟、澳大利亚和中国的批准。
艾伏尼布/ivosidenib的药物疗效:
艾伏尼布/ivosidenib的给药方式
艾伏尼布/ivosidenib的药物相互作用
关于骨髓增生异常综合征
骨髓增生异常综合征 (MDS) 是祖细胞(干细胞)无法成熟为健康血细胞的疾病。在美国,每年报告大约 16,000 例新发 MDS 病例。大约 3.6% 的 MDS 患者存在 IDH1 突变,这被认为是早期“驱动”突变。对于携带 IDH1 突变的 MDS 患者,预后通常与较差的总体结果以及转化为 AML 的风险增加相关。在 TIBSOVO 获批之前,尚无针对该分子定义子集的获批靶向疗法。