

是全球首款口服型XPO1(核输出蛋白)抑制剂。
 老挝卢修斯
老挝卢修斯  用法用量
用法用量 副作用
副作用  注意事项
注意事项  适应症
适应症  药物相互作用
药物相互作用 (1)塞利尼索联合硼替佐米和地塞米松适用于既往至少接受过一种治疗的成年多发性骨髓瘤患者
(2)塞利尼索联合地塞米松适用于治疗复发或难治性多发性骨髓瘤的成人患者,这些患者至少接受过四种先前的治疗,并且对至少两种蛋白酶体抑制剂、至少两种免疫调节剂和一种抗cd38单克隆抗体难治性
(1)塞利尼索适用于治疗复发或难治性弥漫性大B细胞淋巴瘤(DLBCL)的成年患者,包括由滤泡性淋巴瘤引起的至少经过二线系统治疗的弥漫性大B细胞淋巴瘤
(2)本适应症是根据反应率加速批准的,本适应症的继续批准可能取决于确认性试验中对临床益处的验证和描述
(1)与硼替佐米、地塞米松(XVd)联合用药
塞利尼索的推荐剂量为100mg,每周口服一次,每周第1天,直到疾病进展或不可接受的毒性,且与以下药物联合使用:
①硼替佐米1.3 mg/m2,每周第1天皮下给药1次,连续4周,然后暂停1周
②地塞米松20毫克,每周口服两次,每周第1、2天服用
(2)与地塞米松(Xd)联合用药
塞利尼索的推荐剂量为80mg,每周第1天和第3天口服,直到疾病进展或不可接受的毒性,且与地塞米松20mg联合使用
对于硼替佐米、地塞米松详细的使用信息请参考这两个药物的详细说明书
塞利尼索的推荐剂量为每周第1天和第3天口服60mg,直至疾病进展或不可接受的毒性
监测全血细胞计数(CBC)与差异,标准血液化学,体重,营养状况,和容量状态在基线和治疗期间的临床指征,在治疗的前三个月更频繁地监测,评估是否需要调整塞利尼索的剂量以应对不良反应
(1)建议患者在整个治疗过程中保持足够的液体和热量摄入,考虑对有脱水危险的病人进行静脉补水
(2)提供预防性止吐药,在塞利尼索治疗之前和期间给予5-HT3受体拮抗剂和其他抗恶心药物
(1)针对不良反应的剂量调整
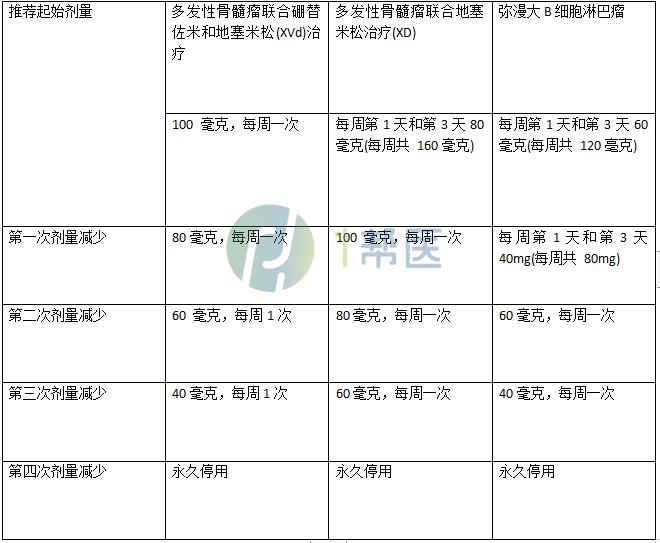
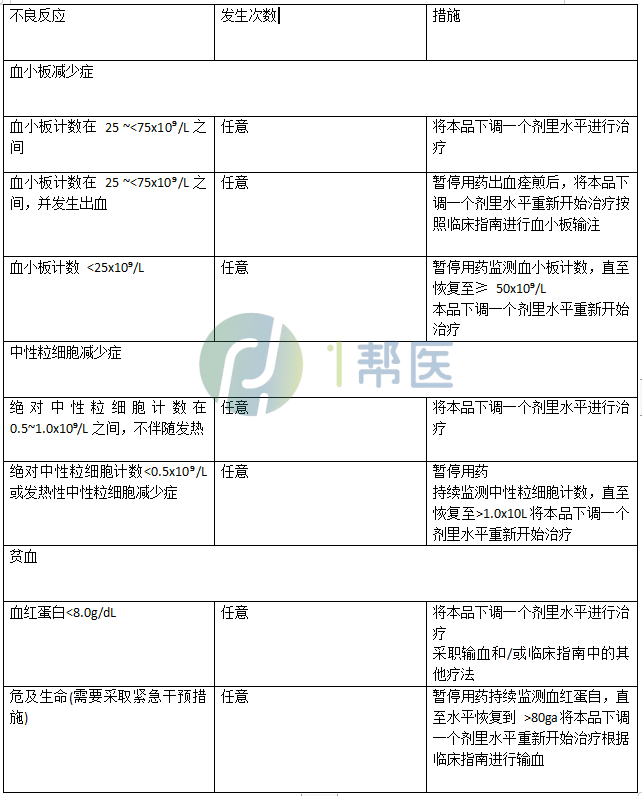
(2)多发性骨髓瘤患者血液不良反应的塞利尼索剂量调整
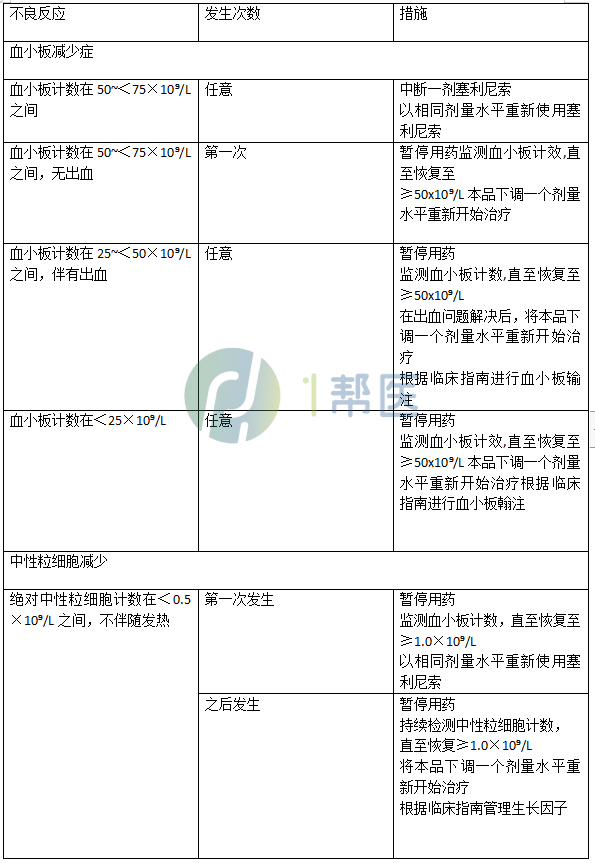
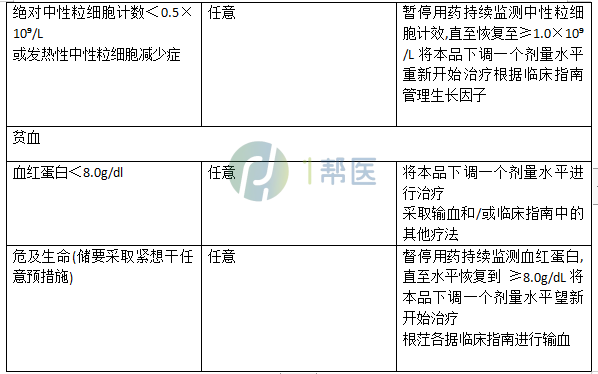
(3)弥漫性大b细胞淋巴瘤患者血液不良反应的塞利尼索剂量调整指南
(4)发生非血液学不良反应时剂量调整
不良反应 | 发生次数 | 措施 |
恶心和呕吐 | ||
1或2级恶心(摄入量下降,但未见显著的体重减轻、脱水或营养不良),或者1级或2级呕吐(每天发生次数 ≤ 5次) | 任意 | 剂量维持,并开始给予其他止吐药 |
3级恶心(热量或液体的口服摄入量不足),或者3级及以上呕吐(每天发生次数≥ 6次) | 任意 | 暂停用药 持续监测,直至恶心或呕吐缓解至≤2级或治疗前水平 开始给予其他止吐药。 将本品下调一个剂量水平重新开始治疗 |
腹泻 | ||
2级(与治疗前相比每日排便增加4 ~ 6次) | 第1次 | 维持用药,并给予支持性治疗 |
第2次及后续 | 将本品下调一个剂量水平 给予支持性治疗 | |
3级及以上(与治疗前相比每日排便增加 ≥ 7次;或需要住院) | 任意 | 暂停用药并给予支持性治疗 持续监测,直至腹泻缓解至 ≤ 2级 将本品下调一个剂量水平重新开始治疗 |
体重下降和厌食 | ||
体重下降10% ~ < 20%之间,或者厌食伴有显著体重下降或营养不良 | 任意 | 暂停用药并给予支持性治疗 持续监测体重,直至恢复到治疗前体重的90%以 上 将本品下调一个剂量水平重新开始治疗 |
低钠血症 | ||
血钠水平 ≤ 130mmol/L | 任意 | 暂停用药,评估并给予支持性治疗 持续监测钠水平,直至恢复至130 mmol/L以上 将本品下调一个剂量水平重新开始治疗 |
疲乏 | ||
2级(持续7天以上)或3级 | 任意 | 暂停用药 持续监测,直至疲乏缓解至1级或治疗前水平 将本品下调一个剂量水平重新开始治疗 |
眼毒性 | ||
2级,白内障除外 | 任意 | 进行眼科评估 暂停用药并给予支持性治疗 监测直至眼部症状恢复至1级或治疗前水平 将本品下调一个剂量水平重新开始治疗 |
≥3级,白内障除外 | 任意 | 终止治疗 进行眼科评估 |
白内障(≥2级) | 任意 | 进行眼科评估 将本品下调一个剂量水平重新开始治疗 监测进展情况 术前24小时和术后72小时暂停用药 |
其他非血液系统不良反应 | ||
3或4级 | 任意 | 暂停用药 持续监测,直至缓解至≤2级,将本品下调一个剂量水平重新开始治疗 |
(1)每次塞利尼索剂量应在一天中大约同一时间服用,每片应用水吞服,不要打碎、咀嚼、压碎或分开药片
(2)如果遗漏或延迟了塞利尼索的剂量,指示患者在下一个常规时间服用下一剂量
(3)如果患者呕吐一剂塞利尼索,患者不应重复剂量,患者应在下一个规定日期服用下一剂
(1)最常见的不良反应(≥20%)是疲劳、恶心、食欲下降、腹泻、周围神经病变、上呼吸道感染、体重下降、白内障和呕吐
(2)3-4级实验室异常(≥10%)为血小板减少症、淋巴减少症、低磷血症、贫血、低钠血症和中性粒细胞减少症
最常见的不良反应(≥20%)是血小板减少、疲劳、恶心、贫血、食欲下降、体重下降、腹泻、呕吐、低钠血症、中性粒细胞减少、白细胞减少、便秘、呼吸困难和上呼吸道感染
(1)最常见的不良反应(发生率≥20%)是疲劳、恶心、腹泻、食欲下降、体重下降、便秘、呕吐和发热
(2)3-4级实验室异常(≥15%)为血小板减少症、淋巴细胞减少症、中性粒细胞减少症、贫血和低钠血症
对本品主要成份或任何辅料过敏者禁用。
密封、30℃以下干燥处保存
成人。儿童、哺乳期妇女及年老体弱者应在医生指导下使用
尚未明确
24个月
片剂
老挝卢修斯
本品主要成份为塞利尼索
20mg片剂为蓝色,圆形,双凸,薄膜包膜,一面有“K20”字样,另一面无任何内容;40mg片剂为蓝色,椭圆形,覆膜,两面都有“X40”字样;50mg片剂为蓝色,椭圆形,覆膜,两面都有“X50”字样;60mg片剂为蓝色,椭圆形,薄膜涂层,两面刻有“X60”字样
(1)塞利尼索可导致血小板减少,导致潜在的致命性出血,注意监测基线、治疗期间和临床显示的血小板计数,在治疗的前两个月提高血小板计数监测频率
(2)根据临床需要进行血小板输注和/或其他治疗
(3)监测病人出血的体征和症状,并及时评估,根据不良反应的严重程度中断和/或减少剂量,或停药
(1)塞利尼索会导致中性粒细胞减少,潜在地增加感染的风险,注意监测基线、治疗期间和临床显示的中性粒细胞计数,在治疗的前两个月提高监测频率
(2)监测患者合并感染的体征和症状,并及时评估
(3)考虑支持性措施,包括针对感染迹象的抗菌剂和生长因子(例如G-CSF)的使用,根据不良反应的严重程度中断和/或减少剂量,或停药
(1)塞利尼索可能会导致胃肠道毒性,通过调整剂量和/或标准止泻剂来控制腹泻,给有危险的患者静脉输液以防止脱水
(2)监测患者在基线、治疗期间和临床指示时的体重
(3)在治疗的前两个月更频繁地监测,通过剂量调整、食欲刺激和营养支持来改善厌食和体重减轻
(1)塞利尼索可引起低钠血症,监测基线、治疗期间和临床指示的钠水平,在治疗的前两个月更频繁地监测
(2)纠正并发高血糖(血清葡萄糖>150 mg/dL)和高血清副蛋白水平的钠水平,根据临床指南(静脉注射盐水和/或食盐片)治疗低钠血症,包括调整饮食
(3)根据不良反应的严重程度中断和/或减少剂量,或停药
(1)本品可引起严重和致命性感染,多数感染与3级或3级以上中性粒细胞减少症无关
(2)本品治疗后报告的非典型性感染包括但不限于真菌性肺炎和疱疹病毒感染
(3)治疗期间监测感染的体征和症状,及时评估和治疗
(1)本品可引起危及生命的神经系统毒性,本品可引起意识模糊状态和头晕
(2)应指导患者避免头晕或意识模糊状态可能引发问题的场合,并指示患者在未得到充分医学建议的情况下,不可服用可能导致头晕或意识 模糊状态的其他药物
(3)建议患者避免驾驶和从事危险职业或活动,如操作重型或潜在危险的机械,直到神经毒性完全消除,优化水合状态、血红蛋白水平和伴随用药,避免加重头晕或精神状态变化,采取适当的跌倒预防措施
(1)基于动物实验获得的数据以及本品的作用机制,孕妇服用本品后可能会对胎儿造成危害
(2)告知孕妇本品对于胎儿的潜在风险,告知育龄女性患者和有生育能力女性伴侣的男性患者,在接受本品治疗期间以及最后一次给药后1周内使用有效的避孕措施
部分患者在接受本品治疗期间发生了新发白内障或白内障恶化,白内障的治疗通常需手术摘除白内障
(以上信息均参考自美国FDA官网塞利尼索说明书英文版 2022.07)
1.如果您发现该药品信息有任何错误,请联系我们修改,我们将热忱感谢您的批评指正!
2.本站所表达的任何关于疾病的建议都不应该被视为医生的建议或替代品,请咨询您的治疗医生了解更多细节。本站信息仅供参考!