摘要:实验组的中位无进展生存期(PFS)为7.8,对照组为5.6,二者的危险比为0.54(0.42,0.71);实验组的中位总生存期(OS)为21.9,比对照组的OS高4.5个月;实验组的客观缓解率(OS)为40.6(35.3,46.0),是对照组的两倍有余。
在HER2CLIMB(NCT02614794)临床试验中评估了图卡替尼(TUKYSA)联合曲妥珠单抗和卡培他滨的疗效,本试验共纳入612名患者。这是一项随机(2:1)双盲安慰剂对照试验。612名患者患有HER2阳性、不可切除的局部晚期或转移性乳腺癌,伴或不伴脑转移,并且之前在新辅助、辅助或转移环境中分别或联合使用曲妥珠单抗(Herceptin、Trastuzumab)、帕妥珠单抗(Pertuzumab、Perjeta)和T-DM1进行治疗。
脑转移患者,包括病变进展或未经治疗的患者,只要神经功能稳定,不需要立即放疗或手术的情况就符合试验条件。该试验排除了软脑膜疾病患者。根据脑转移的存在或病史(是或否)、ECOG的表现状态(0对1)和地区(美国、加拿大或世界其他地区)对随机分组进行分层。
患者在第1个周期的第1天(如有必要)每天两次口服300mg图卡替尼或安慰剂,曲妥珠单抗负荷剂量为8mg/kg,然后在此后的每21天周期的第1天(如有必要)服用维持剂量为6mg/kg的曲妥珠单抗,并在每21天周期的第1天至第14天每天两次口服卡培他滨1000mg/m2。另一种曲妥珠单抗给药方案是在每21天周期的第1天皮下注射600mg曲妥珠单抗。患者接受治疗,直到疾病进展或出现不可接受的毒性。
肿瘤评估,包括基线检查时存在或有脑转移病史的患者的脑部MRI,在前24周每6周进行一次,之后每9周进行一次。
无进展生存率(PFS),采用实体瘤疗效评价标准(RECIST)v1.1进行盲法独立中心评价(BICR)。在所有随机患者中评估其他疗效结果指标,包括总生存率(OS)、有脑转移病史或存在脑转移的患者的PFS(PFSBrainMets)和客观缓解率(ORR)。
实验组的中位无进展生存期(PFS)为7.8,对照组为5.6,二者的危险比为0.54(0.42,0.71);实验组的中位总生存期(OS)为21.9,比对照组的OS高4.5个月;实验组的客观缓解率(OS)为40.6(35.3,46.0),是对照组的两倍有余。
图1:HER2CLIMB试验中无进展生存期(PFS)的Kaplan-Meier分析曲线
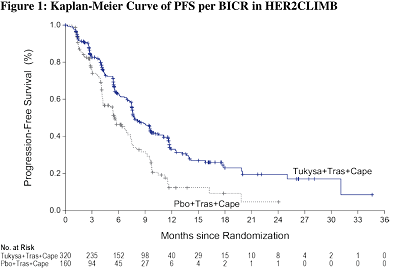
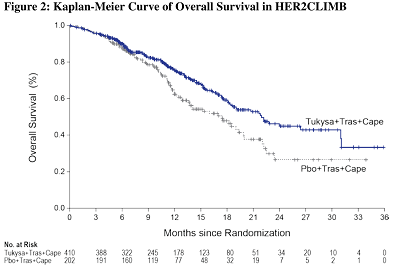
图2:HER2CLIMB试验中总生存率(OS)的Kaplan-Meier分析曲线
 图卡替尼(Tucatinib)
图卡替尼(Tucatinib) 片剂
150mg*30片
 孟加拉珠峰
孟加拉珠峰
口服TKI,治疗HER2阳性乳腺癌,提高2年总生存率
2025-12-27 21:26:45
2025-12-27 21:18:24
2025-12-27 21:12:37
2025-12-27 21:07:01
2025-12-27 21:01:00
2025-08-01 16:04:18
2025-08-01 15:55:41
2025-08-01 15:10:28
2024-12-30 12:13:43
2024-12-30 12:08:02