摘要:Qalsody-首款遗传性渐冻症靶向药物美国FDA获批上市
Qalsody是第四款获FDA批准用于治疗渐冻症的药物,也是治疗遗传性渐冻症的首款药物,那么渐冻症是什么表现?
肌萎缩侧索硬化(ALS)也叫运动神经元病(MND),即常听说的渐冻症。它是上运动神经元和下运动神经元损伤之后,导致包括球部(所谓球部,就是指的是延髓支配的这部分肌肉)、四肢、躯干、胸部腹部的肌肉逐渐无力和萎缩(1)。该病病因至今不明。20%的病例可能与遗传及基因缺陷有关,早期症状不明显,患者可能只感到有无力、肉跳、容易疲劳等症状,渐渐进展为全身肌肉萎缩和吞咽困难,直到呼吸衰竭。
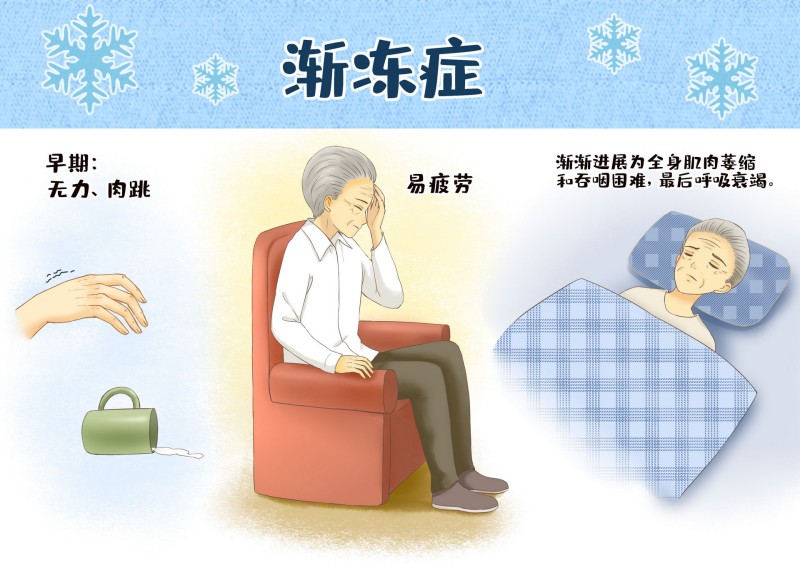
渐冻症被认为与多种基因相关,其中携带SOD1基因突变的患者在渐冻症患者中占了2%,多数携带此基因的病人病情急速发展,起病后生存期不到一年。尚未有针对渐冻症的特效药物,但Qalsody的出现使得这一现象得到了缓解。Qalsody是什么药?它是如何发挥作用的?
Qalsody于2023年4月25日获得了美国FDA的批准在美国上市,用于超氧化物歧化酶1 (SOD1)基因突变的成人肌萎缩性侧索硬化症(ALS)的治疗,并且获得了FDA认证的加速批准和孤儿药名称。
Qalsody是一种反义寡核苷酸,通过与SOD1 mRNA结合引起SOD1 mRNA的降解,从而导致SOD1蛋白合成的减少,来达到治疗疾病的目的。
以上是Qalsody的基本信息,下面就是大家最关心的问题之一,它治疗渐冻症的效果如何?
Qalsody的疗效是在由Timothy M Miller博士带领的一项为期28周的随机、双盲、安慰剂对照临床研究中评估的,研究对象是23至78岁的、由渐冻症引起的虚弱和由中心实验室证实的SOD1突变的患者(NCT02623699)。该试验一共入组了108例患者,按2:1随机分组分别接受Qalsody或安慰剂治疗。主要终点是在预测疾病进展较快的参与者中,渐冻症功能评分表-修订版(ALSFRS-R;范围为0至48,分数越高表示功能越好)总分从基线到第28周的变化。次要终点包括脑脊液(CSF)中SOD1蛋白的总浓度、血浆中神经丝轻链的浓度、慢活能力和16块肌肉的手持测力的变化。试验结果显示:
与安慰剂相比,Qalsody导致脑脊液中SOD1的浓度和血浆中神经丝轻链的浓度降低得更多。在进展较快的亚组中(主要分析),到第28周,Qalsody的ALSFRS-R评分变化为-6.98,安慰剂为-8.14。次要临床终点的结果在两组之间没有显著差异。
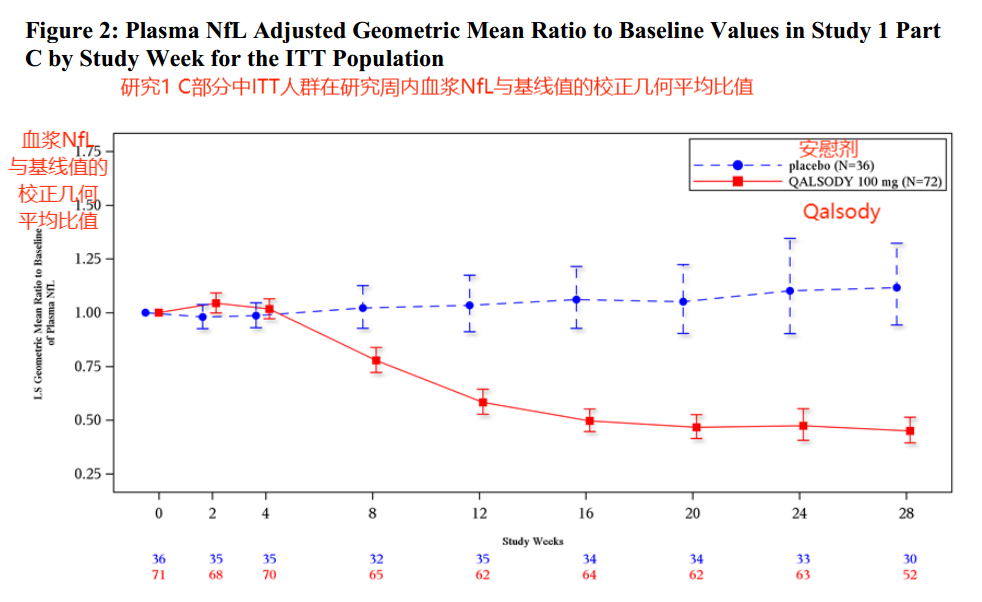
以上结果表示在SOD1型渐冻症患者中,Qalsody在28周内降低了脑脊液中SOD1的浓度和血浆中神经丝轻链的浓度,治疗疾病是有效的(2)。

实验发起者Miller博士曾表示:“对于其他ALS药物研发项目,如果也能如Qalsody一般降低神经丝蛋白轻链的水平,就可以加快确定药物是否有效或其减缓神经退行性疾病进程能力的时间。”Qalsody作为第四款获FDA批准用于治疗渐冻症,首款用于治疗遗传性渐冻症的药物,具体应该如何使用呢?
通过腰椎穿刺术进行鞘内给药,每次给药的推荐剂量为100mg,每隔14天服用3个负荷剂量,此后每28天服用一次维持剂量。
(1)如果错过第二个负荷剂量,请尽快服用,并在14天后服用第三个负荷剂量。
(2)如果错过第三个负荷剂量,请尽快服用,并在28天后服用下一个剂量。
(1)将溶液倒入注射器后,应在室温下立即给药(从药瓶中取出后4小时内),否则单剂量药瓶中任何未使用的内容物都应丢弃。
(2)给药前,用腰椎穿刺针取约10 mL脑脊液,用针头从药瓶中取出所需剂量的15mL,请勿稀释,使用腰椎穿刺针,鞘内推注进行给药,持续1至3分钟。

 Qalsody(tofersen)
Qalsody(tofersen) 注射剂
100mg/15ml
 美国Biogen
美国Biogen
适用于存在肌萎缩侧索硬化的成人患者。
2026-01-13 17:41:16
2025-12-12 23:13:47
2025-12-10 22:39:34
2025-10-28 10:44:29
2025-10-28 09:41:39
2025-10-28 09:39:14
2025-10-12 17:01:38
2025-10-09 16:21:59
2025-10-04 19:55:58
2025-09-22 15:03:09