特立帕肽的主要成分为特立帕肽,它是一种甲状旁腺激素类似物(PTH 1-34)。特立帕肽的作用机制主要是通过模拟甲状旁腺激素(PTH)的作用来调节钙和磷代谢,进而促进骨骼健康。
药品称呼
通用名:特立帕肽
商品名:复泰奥
全部名称:特立帕肽,复泰奥,醋酸特立帕肽/重组人甲状旁腺激素(1-34),醋酸特立帕肽,醋酸特立帕肽52232-67-4,Teriparatide acetate,Teriparatideacetate,Parathyroid Hormone Fragment 1-34 human,Parathyroid Hormone Fragment (1-34),PARATHYROID HORMONE (PTH) HUMAN 1-34,MIN 95%
禁忌
对本品过敏者禁用。
贮藏
应在2°C~8°C的冷藏条件下避光保存。注射笔应在使用后立即放回冰箱。不得冷冻。不得将注射笔在安装有针头的状态下贮藏。
作用机制
特立帕肽[hPTH(1-34)]是一种合成的多肽激素,为人甲状旁腺素PTH的1-34氨基酸片段,该片段是含有84个氨基酸的内源性甲状旁腺素PTH具有生物活性的N-末端区域。
本药的免疫学和生物学特性与内源性甲状旁腺素PTH以及牛甲状旁腺素PTH(bPTH)完全相同。本药刺激骨形成和骨吸收,可减少绝经后妇女骨折的发生率,根据给药方式的不同,还能提高或降低骨密度。
连续输注可导致甲状旁腺素PTH浓度持续增高,因此比仅引起血清甲状旁腺素PTH浓度短暂增高的每日注射法产生的骨吸收作用更强。此外,本药不抑制二磷酸腺苷诱导途径或者胶原诱导途径的血小板聚集反应。
安全与疗效
为研究特立帕肽治疗老年性骨质疏松症患者的骨密度(BMD)和骨标志物的变化,评估生活质量的改善。研究人员选取老年性骨质疏松症患者45例,给予特立帕肽20 μg,每个月注射28 d,疗程12个月。
在治疗前和治疗3,6和12个月分别检测BMD,抽血查生化指标和骨标志物;疼痛数字评分法(NRS)进行疼痛评分;采用简明健康状况调查表(SF-36量表)进行生活质量的评定。
结果,治疗前患者NRS评分为(4.96±2.25)分,治疗3,6及12个月后,患者NRS评分分别为(2.84±1.41),(1.56±1.16),(1.36±1.00)分(P<0.01)。患者治疗后总SF-36评分也较治疗前明显增高(P<0.05)。治疗3,6及12个月,腰椎BMD分别提高约7.7%,12.3%及15.4%;股骨颈BMD提高约3.0%,6.1%及7.6%;股骨粗隆BMD分别提高5.7%,8.6%及10.0%。
治疗3,6和12个月后患者血清骨钙素、骨碱性磷酸酶、Ⅰ型前胶原N-端前肽较治疗前均明显增高(P<0.01),而β型胶原交联C端肽在治疗后12个月有明显降低(P<0.05)。治疗期间副作用少。因此,特立帕肽治疗老年性骨质疏松1年后可明显减轻骨痛,增加腰椎和股骨粗隆BMD,改善患者生活质量。
完整说明书详情:
适应症
适用于有骨折高发风险的绝经后妇女骨质疏松症的治疗。
本品可显著降低绝经后妇女椎骨和非椎骨骨折风险,但对降低髋骨骨折风险的效果尚未证实。
用法用量
本品推荐剂量为每日皮下注射20 微克,注射部位应选择大腿或腹部
应指导患者使用正确的注射方法,本产品为多剂量卡式瓶包装,每天必须使用 指定的笔式注射器进行注射。
本品总共治疗的最长时间为24个月。
病人终身仅可接受一次为期24个月的治疗。
如果膳食不能满足需要,患者应当补充钙和维生素 D。
停止使用本品治疗后,患者可以继续其它骨质疏松治疗方法。
肾功能不全患者:本品不得用于严重肾功能不全患者,有中度肾功能不全患者 应慎用本品。
肝功能不全患者:未在肝功能不全患者中进行研究,应在医生指导下慎用。
儿童及开放性骨骺的青少年:本品尚无在小于 18 岁的儿童和青少年中应用的经验。
不得用于小于18 岁的儿童、青少年和开放性骨骺的青年。
老年用药:无需根据年龄调整剂量。
不良反应
不良反应总结:在接受特立帕肽治疗的患者中最常报告的不良反应有恶心,肢体疼痛,头痛和 眩晕。
不良反应列表:在特立帕肽临床试验中,特立帕肽和安慰剂组中分别有 82.8%和 84.5%的患者 第 2 页/共 11 页报告至少一例不良事件。
下表所列为在治疗骨质疏松的临床研究中和产品上市后,与使用特立帕肽相关的不良反应。
不良反应发生频率的定义如下:十分常见(≥1/10),常见(≥1/100 且<1/10),偶见(≥1/1,000 且<1/100),罕见(≥1/10,000 且<1/1,000),十分罕见 (<1/10,000)。
禁忌
对特立帕肽或本品任何辅料过敏者。
妊娠及哺乳期妇女。
高钙血症患者。
严重肾功能不全患者。
除原发性骨质疏松和糖皮质激素诱导的骨质疏松以外的其他骨骼代谢疾病(包括甲状旁腺功能亢进和Paget's病)。
不明原因的碱性磷酸酶升高。
之前接受过外照射或骨骼植入放射性治疗的患者。
本品的治疗范围应排除骨恶性肿瘤或伴有骨转移的患者。
贮存方法
产品应在 2~8℃的冷藏条件下避光保存。装有药品的注射笔应在使用后立即放回冰箱。不得冷冻。不得将注射笔在安装有针头的状态下贮藏。
适用人群
适用于绝经后妇女。妊娠及哺乳期妇女禁用。儿童、青少年禁用。
药物相互作用
已进行特立帕肽与双氢氯噻嗪的药效相互作用研究,未发现有临床意义的相互作用。
特立帕肽与雷洛昔芬或激素替代治疗合用不会改变特立帕肽对血钙或尿钙的作用,也不改变其临床不良反应。
在一项对15位每天使用地高辛至稳态水平的健康受试者的研究中,特立帕肽单剂量不会改变地高辛对心脏的作用。
然而,有零星病例报告提示,高血钙可能导致患者洋地黄中毒。
由于特立帕肽能瞬时提高血钙水平,因此使用洋地黄的患者应慎用。
有效期
18个月。本品在使用期内的化学、物理及微生物稳定性试验的数据,支持在2~8℃贮藏,使用30天的有效期。 一旦开始使用,本品于2~8℃可贮存30天。如超出上述储存时间和储存条件下使用本品,由使用者负责。
剂型
注射剂
生产厂家
美国礼来Lilly
成分
本品主要成份为特立帕肽
化学结构式:
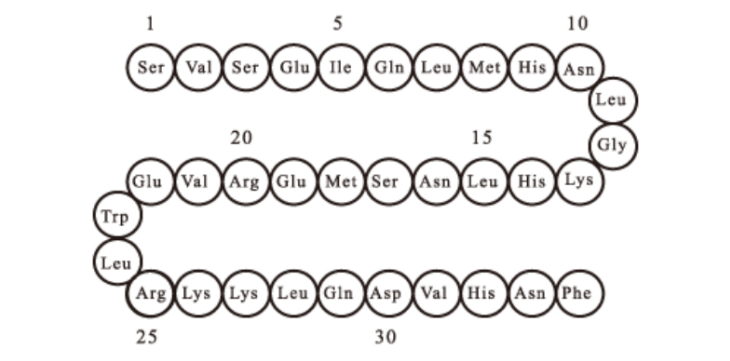
分子式:C181H291N55O51S2
分子量:4117.8 道尔顿
辅料名称:冰醋酸、醋酸钠、甘露醇、间甲酚
性状
本品为无色澄明液体
注意事项
血钙和尿钙
血钙正常的患者注射特立帕肽后发现血钙浓度有一过性的轻微升高。
血钙浓度在注射每剂特立帕肽后4到6小时之间达到峰值并在16到24小时内回到基线水平。
因此如果为了监测血钙而采集血样,应在特立帕肽最近一次注射至少16小时后进行。
在治疗过程中不需要进行血钙的常规监测。
特立帕肽可能导致尿钙排泄量的轻微升高,但在临床试验中高钙尿的发生率与安慰剂相比没有差异。
尿结石
尚未进行特立帕肽在活动性尿石症患者中应用的研究。
因为特立帕肽有加重这种症状的可能,所以在活动性或新发尿石症患者中应慎用。
直立性低血压
在特立帕肽的短期临床研究中,有独立偶发的一过性直立性低血压发作的报告。
典型的报告为在注射4小时内发生并在几分钟至数小时后自行恢复。
一过性直立性低血压发生于最初几次给药时,患者处于俯卧位后可缓解并且不妨碍继续治疗。
肾功能不全
中度肾功能不全的患者应慎用。
肝功能不全
肝功能不全患者应在医生指导下慎用。
青年人群
包括绝经前妇女在内的青年人群中应用特立帕肽的经验有限。
在这类患者中只有获益明显大于风险时才考虑使用特立帕肽。
有生育能力的妇女应在使用特立帕肽时采取有效的避孕措施。
如果怀孕则应停止使用特立帕肽。
治疗期间
对大鼠的研究提示特立帕肽长期给药会使骨肉瘤发生率增加。
在上市后的阶段,发生骨肿瘤和骨肉瘤的病例报道很少。
其与特立帕肽使用的因果关系尚不清楚。
温馨提示
1.如果您发现该药品信息有任何错误,请联系我们修改,我们将热忱感谢您的批评指正!
2.本站所表达的任何关于疾病的建议都不应该被视为医生的建议或替代品,请咨询您的治疗医生了解更多细节。本站信息仅供参考!



 美国礼来Lilly
美国礼来Lilly  在线咨询
在线咨询 
 印度Emcure
印度Emcure
 瑞士诺华
瑞士诺华
 美国艾伯维
美国艾伯维
 三生国健
三生国健 用法用量
用法用量