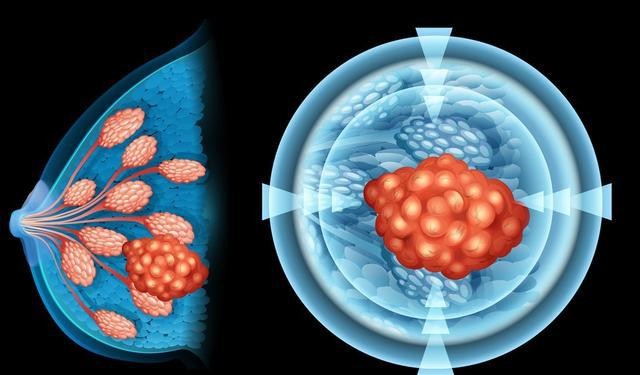
T-DM1,中文名为恩美曲妥珠单抗,商品名为赫赛莱,其英文全称为Ado-trastuzumab emtansine。美国食品药品监督管理局便批准了Kadcyla用于治疗先前接受过曲妥珠单抗(赫赛汀)和/或紫杉类化疗失败的HER2阳性乳腺癌患者。
药品称呼
通用名:T-DM1
商品名称:kadcyla
全部名称:T-DM1,曲妥珠单抗-美坦新偶联物,kadcyla,Ado-trastuzumab emtansine,赫赛莱,恩美曲妥珠单抗
贮藏
1、未使用的样品瓶:在2-8ºC(36-46°F)冷藏
2、重组的小瓶或稀释的溶液
3、冷藏温度为2-8ºC(36-46°F)
4、4小时后丢弃
5、不要冻结
作用机制
Ado-曲妥珠单抗emtansine是一种靶向HER2抗体药物结合物。抗体是人源化抗-HER2 IgG1,曲妥珠单抗。小分子细胞毒素,DM1,是一种微管抑制剂。结合至HER2受体的亚结构区IV,ado-曲妥珠单抗emtansine 进行受体-介导内化和随后溶酶体降解,导致含DM1细胞毒降解产物的细胞内释放。
DM1结合至微管蛋白破坏细胞内微管网络,导致阻止细胞周期和凋亡性细胞死亡。此外,体外研究已证明与曲妥珠单抗相似,ado-曲妥珠单抗emtansine抑制HER2受体信号,介导抗体-依赖细胞介导细胞毒性和抑制过表达HER2人乳癌细胞HER2细胞外结构区的脱落。
安全与疗效
在991例有HER2-阳性,不能切除局部晚期或转移乳癌患者的一项随机化,多中心,开放试验评价KADCYLA的疗效。纳入试验前患者需要以前紫衫烷类和基于曲妥珠单抗治疗。只有既往辅助治疗患者要求在完成辅助治疗期间或6个月内疾病复发。
要求乳腺肿瘤样本在一个中央实验室测定显示HER2过度表达被定义为3+ IHC或FISH扩增比例≥ 2.0。患者被随机分配(1:1)接受拉帕替尼加卡培他滨或KADCYLA。按世界地区(美国,西欧,其他),对不能切除局部晚期或转移疾病(0–1,>1)既往化疗方案数和通过研究者确定内脏相比非内脏疾病随机化分层。
随机化试验证实KADCYLA-治疗组拉帕替尼加卡培他滨-治疗组比较IRC-评估的无进展生存PFS统计显著改善[风险比(HR) = 0.65,95% CI:0.55,0.77,p < 0.0001],而中位PFS增加3.2个月(KADCYLA-治疗组中位PFS为9.6个月相比较在拉帕替尼加卡培他滨组为6.4个月)。见表8和图1。对研究者评估的PFS结果与IRC-评估的PFS相似。
在无进展生存PFS分析时,223例患者已死亡。拉帕替尼加卡培他滨组发生死亡(26%)与KADCYLA组(19%)死亡更多,但是中期总生存OS分析结果不符合预先设定的统计显著性停止边界。在第二次中期总生存OS分析时,已发生331次事件。总生存OS符合共-主要终点;在接受KADCYLA患者总生存OS显著改善(HR =0.68,95% CI:0.55,0.85,p = 0.0006)。
完整说明书详见:
生产厂家
瑞士罗氏
成分
活性成份:恩美曲妥珠单抗
性状
注射用恩美曲妥珠单抗是白色至类白色无菌冻干粉饼,供静脉输注用。
适应症
适用于HER2阳性转移性乳腺癌,既往曾接受曲妥珠单抗和一种紫衫烷类分开或联用患者的治疗。
用法用量
Kadcyla的推荐剂量是3.6mg/kg,静脉输注,每3周1次,直至疾病进展或出现不能耐受的毒性。
禁止用量超过3.6mg/kg,禁止Kadcyla与曲妥珠单抗相互代替使用。
不良反应
最常见的不良反应是疲劳(46%),恶心(43%),血小板减少症(32%),头痛(29%),便秘(27%)。
最常见报告的3或4级事件,除了疲劳(3.2%)外,还有实验室检查异常,血小板减少症(3级,9.3%;
4级,2.4%),血清转氨酶AST(4.3%)或ALT(3.1%)升高,低钾血症(3.3%),以及贫血(2.9%)。
亚洲患者更多的出现3或4级事件,在该类人群中主要是血小板减少症占的频率较高。
T-DM1治疗停药发生在7.0%的患者中,主要是因为实验室检查异常:血小板减少症(1.5%),AST升高(0.8%),和ALT升高(0.5%)。
禁忌
无。
贮存方法
未使用的样品瓶:在2-8ºC(36-46°F)冷藏 重组的小瓶或稀释的溶液 冷藏温度为2-8ºC(36-46°F) 4小时后丢弃 不要冻结
适用人群
适用于HER2阳性转移性乳腺癌,既往曾接受曲妥珠单抗和一种紫衫烷类分开或联用患者的治疗。
有效期
24个月
剂型
注射剂
注意事项
(1)肺毒性:诊断有间质性肺病或肺炎患者中永久终止KADCYLA。
(2)输液相关反应,超敏反应:输注期间和输注后监视体征和症状。
如发生严重输液相关反应或超敏性反应,减慢或中断输液并给予适当医学治疗。
对危及生命输液相关反应永久终止KADCYLA。
(3)出血:在临床试验中发生过致命的出血病例,这些病例并没有已知的确定危险因素、血小板减少症的患者以及正在使用抗凝血和抗血小板治疗的患者。
使用KADCYLA时应注意这些情况,如果必须联合这类药物使用,应提高监测频率。
(4)血小板减少:每次给予KADCYLA前应监测血小板计数。
适当时调整剂量。
(5)神经毒性:监视体征和症状。
对3-4级周围神经病变患者应暂停给药。
(6)HER2检测:使用FDA批准的检验进行检测。
确定HER2阳性转移性乳腺癌患者可给予用药。




 瑞士罗氏
瑞士罗氏  在线咨询
在线咨询 
 英国阿斯利康
英国阿斯利康
 美国Clovis
美国Clovis
 德国拜耳
德国拜耳
 用法用量
用法用量