摘要:厄达替尼-用来治疗尿路上皮癌的FGFR抑制剂
尿路上皮癌是发生于泌尿系统尿路上皮的恶性肿瘤,根据世界卫生组织(WHO)国际癌症研究机构(IARC)提供的最新数据显示,2020年全球膀胱癌新发病例数预计573278例,为全球第十大恶性肿瘤。患者最常表现为无痛性肉眼血尿,伴或不伴尿路刺激征及排尿困难,可能合并发热、盗汗、消瘦等全身症状,同时还可能会存在肿瘤转移引起的相关症状。目前主要治疗方法是以手术治疗为主,晚期患者一般以放疗、化疗为主,对已经耐药或已经发展到晚期的患者,急需新型药物来治疗。此时厄达替尼的问世,就可能延长这类患者的生存时间。
厄达替尼是一种靶向治疗药物,属于酪氨酸激酶抑制剂,是一种具有抗肿瘤活性的药物,其在2019年4月在美国被FDA批准上市使用,也是首个被美国FDA批准的用于口服的FGFR抑制剂。这款药物的适应症主要是针对于携带FGFR3或FGFR2基因突变的铂类化疗后出现疾病进展的局部晚期或转移性尿路上皮癌成人患者,同时也包括新辅助或辅助含铂化疗12个月内的患者。
一项多中心、开放性单臂试验BLC2001(NCT02365597)评估了厄达替尼对治疗转移性尿路上皮癌的疗效,试验共招募了99名局部晚期或转移性尿路上皮癌患者进行试验,试验结果表明,99例晚期FGFR基因突变的患者在接受治疗后,客观缓解率为40%(完全缓解率37%+部分缓解率3%)。
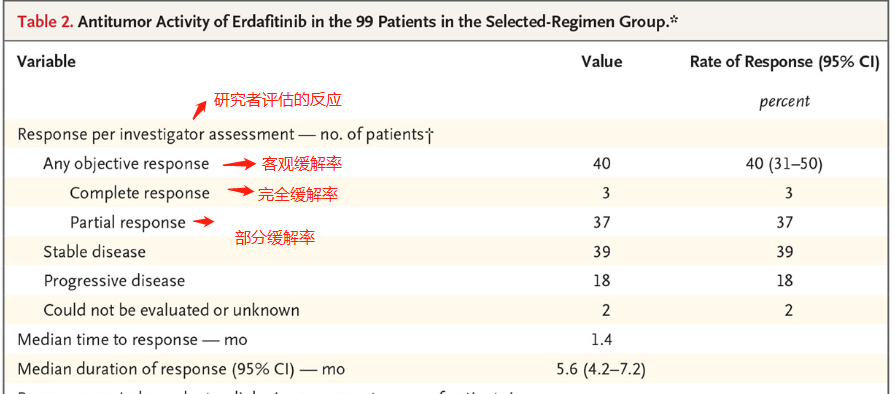
在中位随访11.2个月时,无进展生存期的中位持续时间约为5.5个月,12个月时,无进展生存率为19%(图2A)。在中位随访11个月时,中位总生存期为13.8个月,12个月时,总生存率为55%(图2B)。
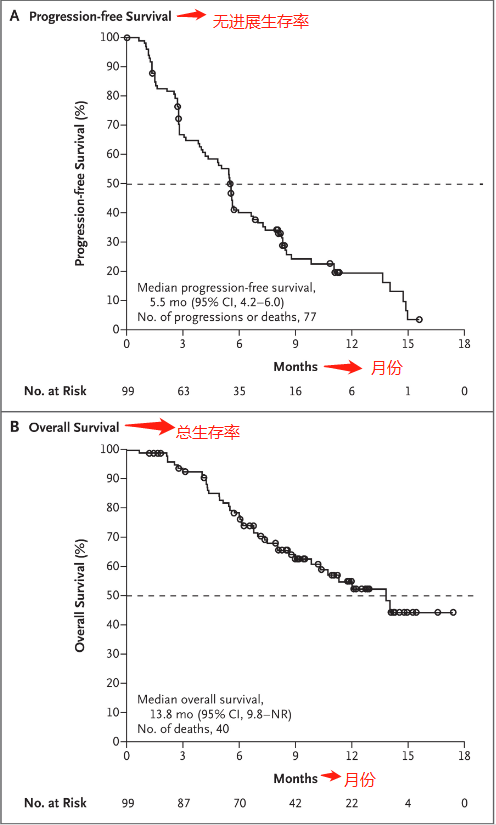
以上试验数据表明,厄达替尼在治疗局部晚期或转移性尿路上皮癌中可以提高客观缓解率,延长患者的生存时间,改善患者的生活质量以及疾病的进展情况,同时对提高患者治疗疾病的信心也有一定帮助,此外该试验数据也表明厄达替尼对治疗尿路上皮癌有显著疗效。
作为一种靶向治疗药物,服用厄达替尼会出现什么不良反应呢?小编帮助大家查询了一下,目前最常见的不良反应包括口炎、疲劳、腹泻、口干、指甲紊乱、食欲下降、味觉障碍、皮肤干燥、干眼、脱发、足底红肿综合征、便秘、腹痛、恶心、肌肉骨骼疼痛等,同时还会存在一些实验室的异常(发生率≥20%)如磷酸盐升高、肌酐升高、丙氨酸转氨酶升高、钠降低、血红蛋白降低、天门冬氨酸转氨酶升高、镁降低、钙增加等。
1、一般情况下,药物应每日一次,一次8mg,直接口服,根据血清磷酸盐(PO4)水平和14至21天的耐受性,剂量增加至9mg,每日一次。
2、整片吞下,伴随或不伴随食物,如果服用本药后任何时间出现呕吐,应在第二天服用下一剂。
3、治疗应持续至疾病出现进展或发生不可接受的毒性。
4、由于使用本品时可能会导致眼部疾病,因此所有患者均应根据需要使用眼镇痛药进行干眼预防。
5、治疗之前4个月需要每月进行一次眼科检查,治疗后每3个月进行一次眼科检查,并随时紧急检查视力症状。
6、由于服用本品可能会出现胚胎毒性,因此建议有生育潜力的女性伴侣的男性患者在本药治疗期间和最后一次给药后一个月内使用有效的避孕措施。
FGFR靶点作为目前“不限癌种”的热门靶点之一,FGFR抑制剂上市后的适应症不仅体现在尿路上皮癌上,还体现在胆管癌上,除此之外,该靶点还覆盖了超过16种癌种,主要包括胃癌、肺癌等实体瘤。2022年美国临床肿瘤学会(ASCO)年会上,杨森公司公布了FGFR激酶抑制剂治疗具有FGFR突变基因的晚期实体瘤患者的治疗效果。
该疗法不区分肿瘤位置或组织学形态,中期分析是基于178位带有32种不同组织学形态肿瘤病患的结果。在截止日期,根据独立评审委员会(IRC)的标准评估疗效,客观缓解率为29.2%,疾病控制率为72.5%,此研究还发现厄达替尼在14中实体瘤中有效果。
目前,厄达替尼还未能在中国上市,因此患有局部晚期或转移性尿路上皮癌的患者需要应用此药物可能要通过海外代购或者直接到国外进行购买。
由于FGFR抑制剂对其相关的癌症有较好疗效,因此发展FGFR靶向抗肿瘤药物对于癌友来说是一件好事。
 厄达替尼(Erdafitinib)
厄达替尼(Erdafitinib) 片剂
3mg*28粒|4mg*28粒|5mg*28粒
 老挝卢修斯
老挝卢修斯
有FGFR3或FGFR2基因突变的、在至少一种先前的铂类化疗方案进行中或化疗后出现疾病进展,包括新辅助或辅助铂类化疗方案治疗的12个月内的局部晚期或转移性尿路上皮癌的成人患者。
2025-10-01 20:15:49
2025-10-01 20:13:56
2025-10-01 19:02:00
2025-10-01 19:00:46
2026-03-17 22:26:02
2026-03-17 22:06:52
2026-01-15 13:55:13
2026-01-15 13:47:42
2026-01-15 11:56:27
2026-01-15 11:40:40