摘要:Epkinly治疗大B细胞淋巴瘤获批,完全缓解率达39%!
2023年5月,美国艾伯维(Abbvie)宣布,美国FDA批准了双特异性抗体疗法Epkinly上市,用于治疗既往接受过二线或多线(≥2)系统治疗后的复发或难治性弥漫性大B细胞淋巴瘤(R/R DLBCL)患者,这也是首款获得FDA批准的治疗大B细胞淋巴瘤患者的双特异性抗体疗法。

大B细胞淋巴瘤是一种来源于B细胞的恶性淋巴瘤,其在非霍奇金淋巴瘤中的比例高达40%-50%。一般情况下,大B细胞淋巴瘤的治疗是比较好的,对于早期的病人,可以进行免疫化疗,再加上稳固的放疗,长期治愈率在70%-80%之间。而对晚期大B细胞淋巴瘤,如果能进行6-8个疗程的靶向免疫化疗,或继续进行自体造血干细胞,总生存率可达40-60%。目前有很多的新药已经上市,针对大B细胞淋巴瘤都取得了较好的疗效。
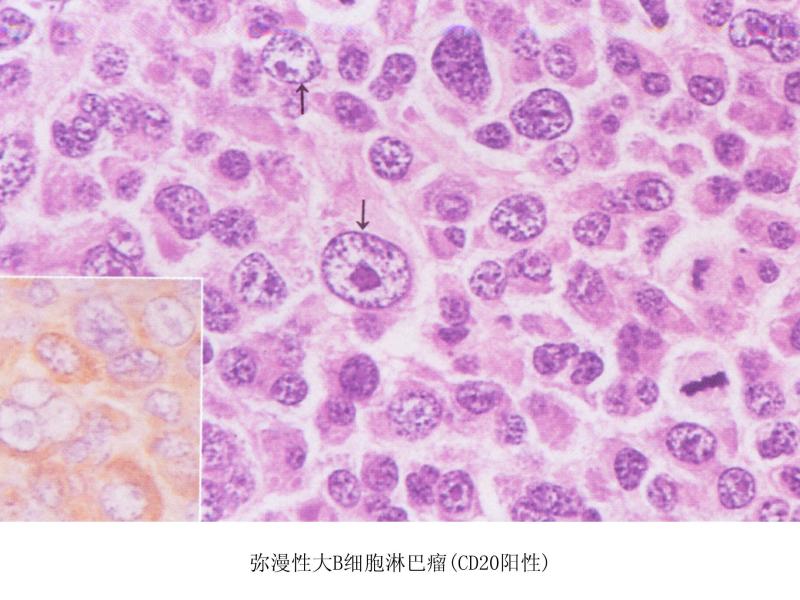

Epkinly是第一个也是唯一一个针对该适应症的T细胞结合双特异性抗体。该药属于IgG1型双特异性单克隆抗体,通过与T细胞表面的CD3及B细胞表面的CD20相结合,激活T细胞表面的CD3及B细胞表面的CD20,发挥免疫抑制作用。
该药具体适用于治疗复发或难治性弥漫大B细胞淋巴瘤(DLBCL)的成人患者,包括惰性淋巴瘤引起的复发或难治性弥漫大B细胞淋巴瘤,以及两种或两种以上系统治疗后的高级别B细胞淋巴瘤。
使用本品时需要特别注意以下事项:
1、使用本品期间多饮水,并且本品只能皮下注射。
2、在第1周期的每次给药前预先用药。
3、EPKINLY 只能由合格的医疗保健专业人员在适当的医疗支持下使用,以控制严重反应,如细胞因子释放综合征(CRS)和免疫效应细胞相关神经毒性综合征(ICANS)。
4、根据表1中的给药方案进行皮下注射,以降低细胞因子释放综合征(CRS)的发生率和严重程度,由于细胞因子释放综合征(CRS)和免疫效应细胞相关神经毒性综合征(ICANS)的风险,患者应在第1周期第15天使用48mg剂量后住院24小时。
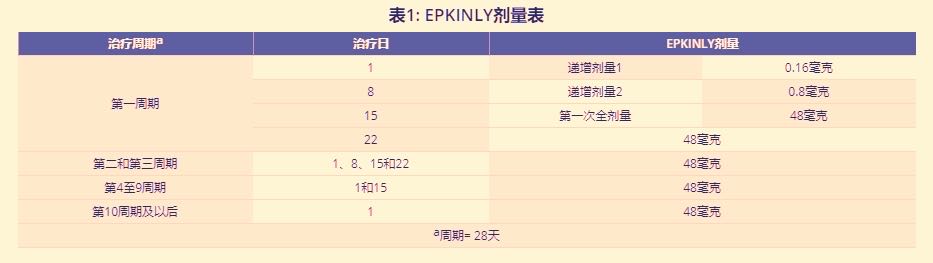
此次Epkinly新适应症的获批是基于1/2期EPCORE NHL-1研究的结果,该试验共有148名患者入组,旨在评估Epkinly的初步疗效和安全性,研究的主要疗效终点为客观缓解率(ORR)。
试验结果证明,Epkinly的客观缓解率(ORR)为63.1%,完全缓解率(CR)在38.9%。也就是说100名患者中有39名患者得到了疾病的完全控制(见下图)。
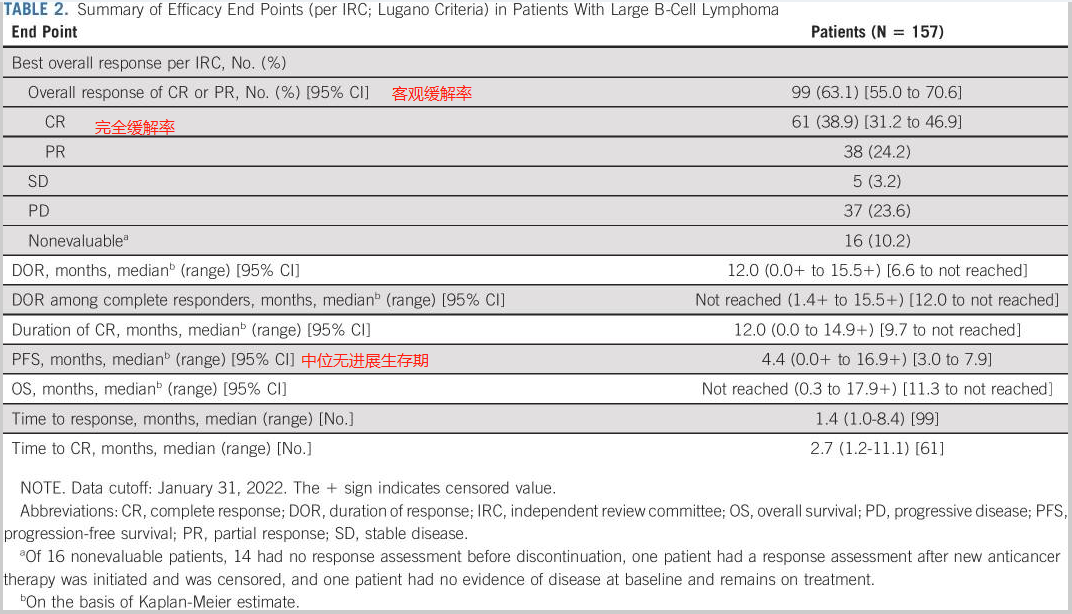
由以上试验数据可知,皮下注射Epkinly在治疗复发或难治性大B细胞淋巴瘤患者中实现了快速、深度和持久的反应,也侧面映证了Epkinly的疗效。
目前除Epkinly外,关于治疗大B细胞淋巴瘤的药物还有25种,已经上市的有4种,目前申请上市的有3种,处于临床3期阶段的有1种,处于临床1期的药物有5种,在临床2期的药物目前也有5种,处于临床2/3期的药物有2种,处于临床1/2期的药物有4种,处于临床1期的药物有5种,处于临床申请阶段的药物有2种,处于临床前阶段的药物有1种。由于篇幅问题,今天在这里为大家介绍两种已经上市的药物,其他药物后续会为大家详细介绍,感兴趣的可以持续关注。

该药属于CD19调节剂,2021.9月在中国审批下上市,瑞基奥仑赛注射液此次获批的适应症为:用于治疗经过二线或以上系统性治疗后成人患者的复发或难治性大B细胞淋巴瘤(r/r LBCL),瑞基奥伦赛是中国获得批准的第二个CAR-T药物,同时也是中国第一个用于一类生物制剂的CAR-T药物。
该药同样属于CD19调节剂,除此之外还是T淋巴细胞替代物,2021.2月份在美国上市,被美国和欧盟批准为“孤儿药”。该药的在研适应症除大B细胞淋巴瘤外,还有B细胞慢性淋巴细胞白血病、非霍奇金淋巴瘤等。

 艾可瑞妥单抗Epkinly
艾可瑞妥单抗Epkinly 注射剂
4mg/0.8ml| 8mg/0.8ml
 美国艾伯维
美国艾伯维
适用于治疗复发或难治性弥漫性大B细胞淋巴瘤(DLBCL)的成年患者
2026-03-17 22:26:02
2026-03-17 22:06:52
2026-01-15 13:55:13
2026-01-15 13:47:42
2026-01-15 11:56:27
2026-01-15 11:40:40
2026-01-15 11:36:02
2026-01-14 20:52:28
2026-01-14 20:46:25
2026-01-14 20:33:22