摘要:试验概括赫赛莱(KADCYLA,T-DM1)在转移性乳腺癌中的疗效是在一项随机、多中心、开放标签试验(EMILIA)(NCT00829166)中评估的,共有991名her2阳性、不可切除的局部晚期或转移性乳腺癌患者参加。在试验登记前需要既往紫杉烷和曲妥珠单抗为主的治疗。仅接受过辅助治疗的患者在完成辅助治疗的6个月内必须有疾病复发。试验内容患者被随机分配(1:1)接受拉帕替尼加卡培他滨或赫赛莱治疗。
赫赛莱(KADCYLA,T-DM1)在转移性乳腺癌中的疗效是在一项随机、多中心、开放标签试验(EMILIA)(NCT00829166)中评估的,共有991名her2阳性、不可切除的局部晚期或转移性乳腺癌患者参加。在试验登记前需要既往紫杉烷和曲妥珠单抗为主的治疗。仅接受过辅助治疗的患者在完成辅助治疗的6个月内必须有疾病复发。
患者被随机分配(1:1)接受拉帕替尼加卡培他滨或赫赛莱治疗。赫赛莱在21天周期的第1天以3.6mg/kg静脉滴注。拉帕替尼以1250mg/d口服,每天1次,21天周期,卡培他滨以1000mg/m2口服,每天2次,在21天周期的第1-14天。患者接受赫赛莱或拉帕替尼加卡培他滨治疗,直到疾病进展、撤销同意或不可接受的毒性。
在初步分析时,赫赛莱使用研究药物的中位时间为5.7个月(范围:0-28.4),lapatinib为4.9个月(范围:0-30.8),卡培他滨为4.8个月(范围:0-30.4)。该研究的共同主要疗效结果是基于独立评审委员会(IRC)的肿瘤反应评估的无进展生存期(PFS)和总生存期(OS)。PFS定义为从随机分组之日到疾病进展或任何原因死亡之日(以较早发生者为准)的时间。总生存期定义为从随机分组之日到任何原因导致死亡之日的时间。其他结果包括PFS(基于研究者的肿瘤反应评估),客观缓解率(ORR),缓解持续时间和症状进展时间。
随机试验显示,与拉帕替尼+卡培他滨治疗组相比,赫赛莱治疗组在IRC评估的PFS方面有显著的统计学改善[风险比(HR)=0.65,95%CI:0.55,0.77,p<0.0001],中位PFS增加了3.2个月(赫赛莱治疗组中位PFS为9.6个月,而拉帕替尼+卡培他滨组为6.4个月),见图1。研究者评估的PFS的结果与IRS评估的PFS相似。
图1:IRC评估EMILIA试验中无进展生存(PFS)的Kaplan-Meier曲线分析结果如下:
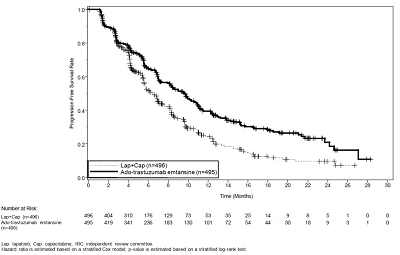
注:虚线表示拉帕替尼+卡培他滨(n=496);实线表示赫赛莱(n=495)
2026-03-17 22:06:52
2026-01-15 13:55:13
2026-01-10 15:15:05
2026-01-10 15:00:56
2026-01-08 21:08:49
2026-01-08 10:38:32
2026-01-08 02:03:54
2026-01-08 01:51:01
2026-01-08 01:45:38
2026-01-06 22:26:45