摘要:ZAVZPRET鼻腔喷雾剂被美国FDA批准用于成人偏头痛治疗
偏头痛是一种以严重头疼发作为特征的神经系统疾病,持续时长可达4-72小时,伴有中度至重度搏动性头痛症状,导致恶心、呕吐或声音和光敏感(畏声和畏光)。据估计,在全球范围内,每年有超过500万人受到偏头痛困扰。目前,世界卫生组织(WHO)将偏头疼列为世界第二大致残原因,并正在积极致力于开发更有效、更安全的治疗方法来帮助治疗偏头痛。但目前的临床数据表明,有近40%的偏头痛患者在接受急性疗法治疗时的疗效不尽人意。
在这种情形下,3月10日,FDA批准Zavegepant上市,成为首个且唯一一个通过鼻内给药的CGRP受体拮抗剂,在偏头痛治疗领域开启非口服CGRP靶向药物治疗新时代。Zavegepant的问世可谓是暗室逢灯,为无数饱受偏头痛困扰的患者带来了福音。
Zavegepant是一种第三代高亲和力、高选择性的小分子CGRP受体拮抗剂。CGRP是一种血管舒张神经肽,全名为降钙素基因相关肽(calcitonin gene-related peptide),被认为是与偏头痛相关的病理因素。Zavegepant的特异性结合能力非常强,可以有效地阻断CGRP受体,从而抑制 CGRP神经肽的生物活性,从而抑制偏头痛的发作。
Zavzpret(zavegepant)之所以能够被FDA批准上市,是因为其在两项临床试验中表现出的疗效。在两项关键、随机双盲、安慰组为对照的试验;Zavzpret在此两项试验中,均达成了共同主要终点——疼痛缓解与MBS(most bothersome symptom)缓解。
首先,一项Ⅱ/Ⅲ期临床试验(NCT03872453)的结果显示,接受10mg、20mg Zavzpret治疗2小时后,使用Zavzpret(zavegepant)的患者分别有22.5%、23.1%的患者实现头痛缓解,而安慰剂组该数值为15.5%,达到主要疗效终点。
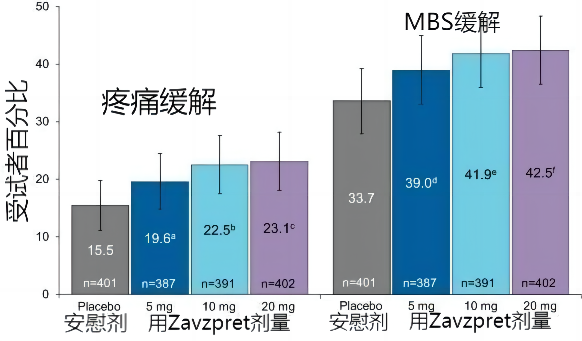
而发布于《柳叶刀》子刊Lancet Neurology的Ⅲ期临床试验(NCT04571060)也同样达到了共同主要终点,结果显示,治疗治疗两小时后,使用Zavzpret(zavegepant)的患者达到疼痛缓解患者比例24%,而安慰剂组仅有 15%。另外在使用Zavzpret(zavegepant)的患者中有40%没有出现MBS(most bothersome symptom)。
除了对偏头痛患者治疗方面的积极成果,Zavzpret(zavegepant)的获批上市也有望为偏头痛市场的繁荣注入新活力。我们也期待在未来,作为偏头痛患病人数最多的国家,我们会有越来越多的国内药企参与到针对偏头痛的CGRP靶点药物研发中去,带动我国乃至全球偏头痛治疗领域的进步。
辉瑞全球生物医药业务总裁兼首席商务官Angela Hwang女士表示:“Zavzpret的获批上市,无疑将帮助更多的偏头痛患者,尤其是那些倾向口服药物以外其它治疗选择的患者。辉瑞将继续开发偏头痛疗法,以进一步支持全球受这种衰弱性疾病影响的数十亿患者。”


 Zavzpret(zavegepant)
Zavzpret(zavegepant) 喷雾剂
10mg
 美国辉瑞
美国辉瑞
偏头痛的成人患者。
2023-03-27 15:26:34
2023-03-27 16:44:11
2026-03-17 22:26:02
2026-03-17 22:06:52
2026-01-15 13:55:13
2026-01-15 13:47:42
2026-01-15 11:56:27
2026-01-15 11:40:40
2026-01-15 11:36:02
2026-01-14 20:52:28