摘要:ADC药物引领精准靶向治疗,DS8201实力雄厚早于20世纪初,一位德国学者就已提出“魔法子弹”这一概念,这是抗体药物偶联物(ADC)药物最早的起源。ADC药物是将单克隆抗体作为载体,通过连接子偶联小分子细胞毒性药物,以实现对肿瘤细胞的精准靶向治疗,从而特异性杀伤肿瘤细胞,并减少药物对正常细胞的毒性损伤。相较于传统细胞毒性药物,此类药物具有毒副作用小、靶向性强等特点,在临床上具有良好的治疗潜力。A
早于20世纪初,一位德国学者就已提出“魔法子弹”这一概念,这是抗体药物偶联物(ADC)药物最早的起源。ADC药物是将单克隆抗体作为载体,通过连接子偶联小分子细胞毒性药物,以实现对肿瘤细胞的精准靶向治疗,从而特异性杀伤肿瘤细胞,并减少药物对正常细胞的毒性损伤。相较于传统细胞毒性药物,此类药物具有毒副作用小、靶向性强等特点,在临床上具有良好的治疗潜力。

目前,此类药物的研究已进展到第三代,2019年12月在美上市的DS8201(Enhertu、优赫得)被誉为“最强ADC药物”,该药现已有四项适应症获得美国药监局(FDA)批准,下面就请跟随小编一起来了解下DS8201强大的“疗效魔力”吧!
DESTINY-Breast03试验纳入了524例既往接受过曲妥珠单抗和紫杉醇治疗,或在辅助治疗期间及治疗后6个月内出现复发的HER2阳性、不可切除和/或转移性乳腺癌患者,旨在比较恩美曲妥珠单抗(trastuzumab emtansine)和DS8201的疗效和安全性。
结果显示,DS8201组的无进展生存期(PFS)为28.8个月,对照组仅为6.8个月,接受DS8201治疗的患者无进展生存期是接受恩美曲妥珠单抗的4倍以上。对照组的中位总生存期(OS)仅为6.8个月,而DS8201组的中位总生存期尚未达到,这意味着接受DS8201治疗的患者的生存时间更长。
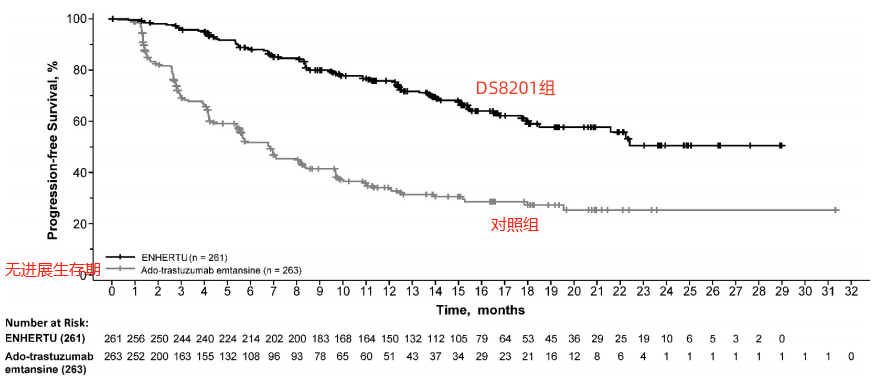
安全性上,DS8201组和对照组≧3级治疗相关的不良反应的发生率基本一致,分别为56%和52%,并且两组均未发生4级-5级不良反应。
研究证实相较于恩美曲妥珠单抗,DS8201治疗HER2阳性转移性乳腺癌患者显著延长患者的生存时间,改善无进展生存期,这表明DS8201的疗效持续时间更持久,且安全性可控。目前DS8201已成为治疗既往接受过抗HER2治疗的、HER2阳性不可切除或转移性乳腺癌成人患者的二线治疗标准方案。
2022年《新英格兰医学杂志》公布了DESTINY-Breast04试验的结果,该试验比较了DS8201和化疗用于既往接受过一线或二线化疗的HER2低表达转移性乳腺癌患者的疗效和安全性。
结果显示,DS8201组的中位无进展生存期为9.9个月,化疗组为5.1个月,接受DS8201治疗的患者无进展生存期是接受化疗的近2倍。两组的中位总生存期分别为23.4个月和16.8个月,DS8201组患者的生存时间显著长于化疗组患者,并且DS8201组相较于化疗组,患者死亡风险降低36%。
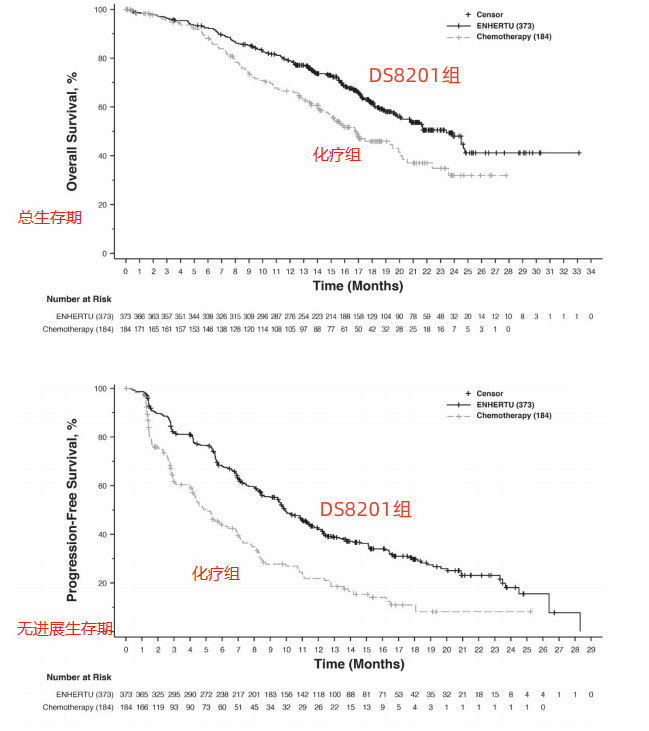
安全性上,DS8201治疗的患者中有52.6%发生≧3级不良反应,低于化疗组的67.4%,但DS8201组中有12.1%的患者发生治疗相关的间质性肺疾病或肺炎。
该研究发现相较于化疗,DS8201显著改善了HER2低表达不可切除或转移性乳腺癌患者的无进展生存期和生存时间。乳腺癌中约有一半患者为HER2低表达,HER2阳性约有20-30%,DS8201对这两种亚型的乳腺癌均表现出良好的疗效,这意味着该药在乳腺癌的治疗中占有举足轻重的地位。
在DESTINY-Lung01试验中,已证实DS8201对既往接受过治疗的HER2突变非小细胞肺癌患者具有持久的治疗活性,随后研究人员开展了DESTINY-Lung02试验,进一步评估了DS8201剂量为5.4mg/kg(低剂量组)和6.4mg/kg(高剂量组)时,患者的临床获益情况和安全性。
其中期分析显示,低剂量组和高剂量组患者的客观缓解率分别为53.8%和42.9%,但高剂量组治疗乳腺癌患者不良反应的发生率更高,高剂量组≥3级治疗相关的不良反应发生率为58%,低剂量组仅为31.7%。
DESTINY-Lung02试验表明,无论是高剂量还是低剂量,DS8201在既往接受过治疗的HER2突变的非小细胞肺癌患者中均具有显著的临床活性,但剂量为5.4mg/kg的DS8201治疗安全性更佳。基于以上试验数据,2022年8月11日FDA加速批准了DS8201用于治疗不可切除或转移性的HER2突变非小细胞肺癌成人患者。
DESTINY-Gastric01试验旨在比较DS8201和化疗,在既往接受过包含曲妥珠单抗在内的二种化疗后进展的、局晚期或转移性HER2阳性胃或胃食管交界处腺癌患者中的疗效和安全性。
结果显示,DS8201组的客观缓解率为51%,化疗组仅为14%,接受DS8201治疗的患者客观缓解率约是化疗的3.6倍。DS8201组和化疗组的中位总生存期分别为12.5个月和8.4个月,接受DS8201治疗的患者生存时间也显著长于化疗组。
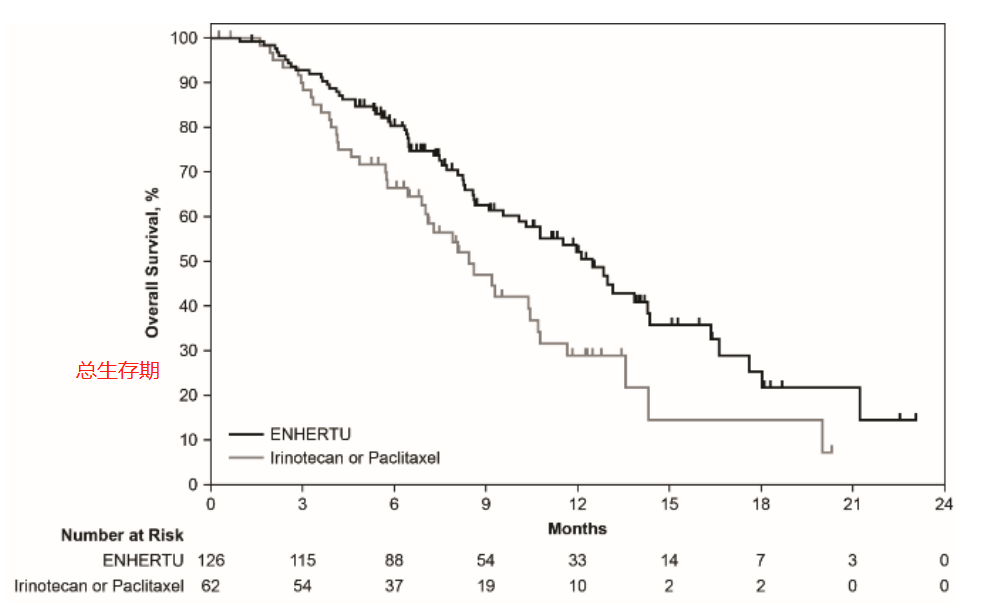
安全性方面,治疗期间最常见的≥3级不良反应为中性粒细胞计数减少、贫血、白细胞计数减少,但以上不良反应的发生率DS8201组均高于化疗组。
该试验表明,与标准化疗相比,DS8201可显著改善HER2阳性胃癌患者的客观缓解率和总生存期,但该药的安全性欠佳,具有显著的骨髓抑制。2021年1月15日,DS8201获美国药监局批准适用于既往接受过曲妥珠单抗的HER2阳性局晚期或转移性胃或胃食管交界处腺癌患者,这一举措为化疗效果不佳的胃癌患者提供了新选择。
因DS8201在乳腺癌、肺癌和胃癌中具有良好的临床活性,这掀起了DS8201治疗其他癌症的研究热潮。在DESTINY-CRC01试验中,DS8201用于HER2阳性结直肠癌,患者的中位无进展生存期和总生存期分别为6.9个月和15.5个月,而疾病控制率甚至高达83%,这进一步证实DS8201具有治疗多种癌症的潜力。目前尚无ADC药物获批用于治疗HER2阳性结直肠癌,而DS8201或将开启结直肠癌治疗新篇章!
 优赫得/德曲妥珠单抗(DS8201)
优赫得/德曲妥珠单抗(DS8201) 冻干粉
100mg
 英国阿斯利康
英国阿斯利康
靶向HER2的抗体和拓扑异构酶抑制剂的药物偶联物。
2025-10-01 18:01:43
2025-10-01 17:53:46
2025-10-01 17:19:20
2025-10-01 17:13:44
2025-10-01 17:05:17
2025-10-01 17:00:56
2025-10-01 16:47:52
2025-10-01 16:22:20
2025-05-22 14:49:28
2025-05-22 14:39:38