摘要:维利西呱在国内获批上市2022年5月18日,中国药品监督管理局批准了拜耳公司心力衰竭的新药-维利西呱(中文名:维可同 英文名:Verquvo)的申请,维利西呱-心衰新药在国内获批上市
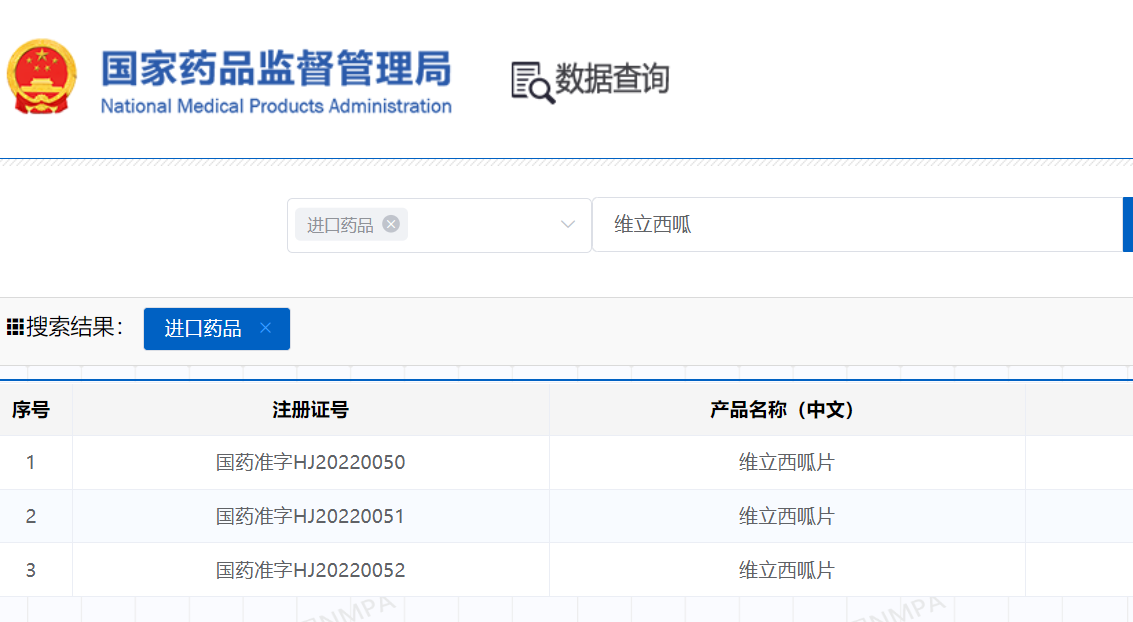
2022年5月18日,中国药品监督管理局批准了拜耳公司心力衰竭的新药-维利西呱(中文名:维可同 英文名:Verquvo)的申请,此次申请包括三种剂量,分别是2.5mg、5mg、10mg。该药作为首个用于心衰治疗的sGC刺激剂上市。
维利西呱是可溶性鸟苷酸环化酶(sGC)的刺激物,sGC是一氧化氮(NO)信号通路中的一种重要酶。当NO与sGC结合时,该酶催化胞内环鸟苷(cGMP)的合成,cGMP是在血管张力、心脏收缩力和心脏重塑的调节中发挥作用。维利西呱通过直接刺激sGC,独立于NO并与NO协同,增加细胞内cGMP水平,导致平滑肌松弛和血管舒张,最终达到治疗心衰的效果。(1)
2021年对几项里程碑性试验的新分析发现,联用不同作用机制的抗心衰药物越多,患者预后越佳 (2) ,这提示, 多机制共同治疗或是突破心衰治疗瓶颈的关键,而目前标准药物治疗主要针对神经、内分泌机制(3)。在试验中,证实了在标准治疗的基础上,维立西呱能够进一步降低心血管死亡和因心衰住院的绝对风险4.2%,因为本研究中包括的患者住院或死亡的风险很高,这被认为是显着的。因此,在充分标准治疗的基础上联合维立西呱,可显著降低患者心血管死亡或因心衰住院风险,进一步改善预后(4)。维利西呱作为首个sGC刺激剂,开启了治疗心衰“细胞-信号通路”的大门,标志着心衰治疗有了新的格局。
该试验是一项随机、平行组、安慰剂对照、双盲、事件驱动、多中心的试验。在5050名有症状的慢性心力衰竭(纽约心脏协会[NYHA]II-IV级)和左心室射血分数(LVEF)低于45%(正常范围在50%-70%)的成年患者中,使用维利西呱和安慰剂进行比较。心力衰竭恶化事件被定义为在随机化前6个月内住院或在随机化前3个月内因心力衰竭使用门诊静脉利尿剂。
患者被随机分配接受维利西呱10毫克或相应的安慰剂。维利西呱的起始剂量为:每天一次,每次2.5毫克,然后以大约2周的间隔增加到每天一次,每次5毫克,以及目标剂量每天一次,每次10毫克(视患者耐受情况而定)。安慰剂的剂量也作了类似的调整。大约1年后,两组中90%的患者都接受了10毫克目标剂量的治疗。
在研究过程中,与安慰剂相比,维利西呱的年化绝对风险降低(ARR)为4.2%。第四列为绝对风险度,降低了4.20%。在入院总人数方面:维利西呱组35.5%<38.5%安慰剂组。
这意味着,服用维利西呱后,患者因心血管死亡和心衰入院的风险降低,死亡和入院总人数降低。
在全因死亡率和心衰入院总人数方面:维利西呱37.9%<40.9%组安慰剂组。
这意味着,服用维利西呱后,患者因任何原因死亡和心衰入院的人数降低,得到了收益。
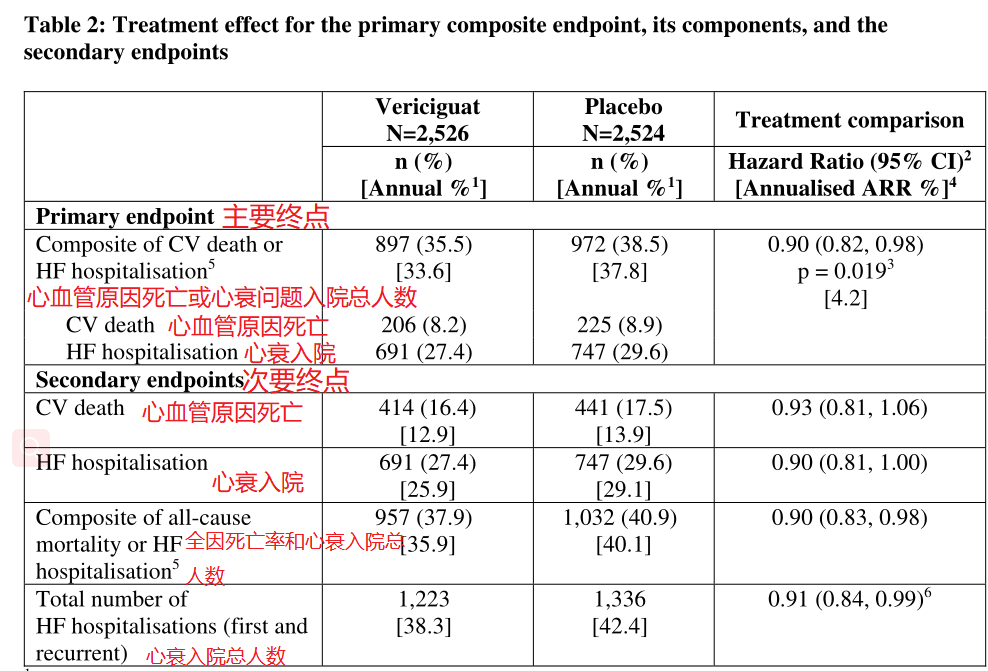 图为欧洲药监局维利西呱说明书中治疗心衰疗效数据
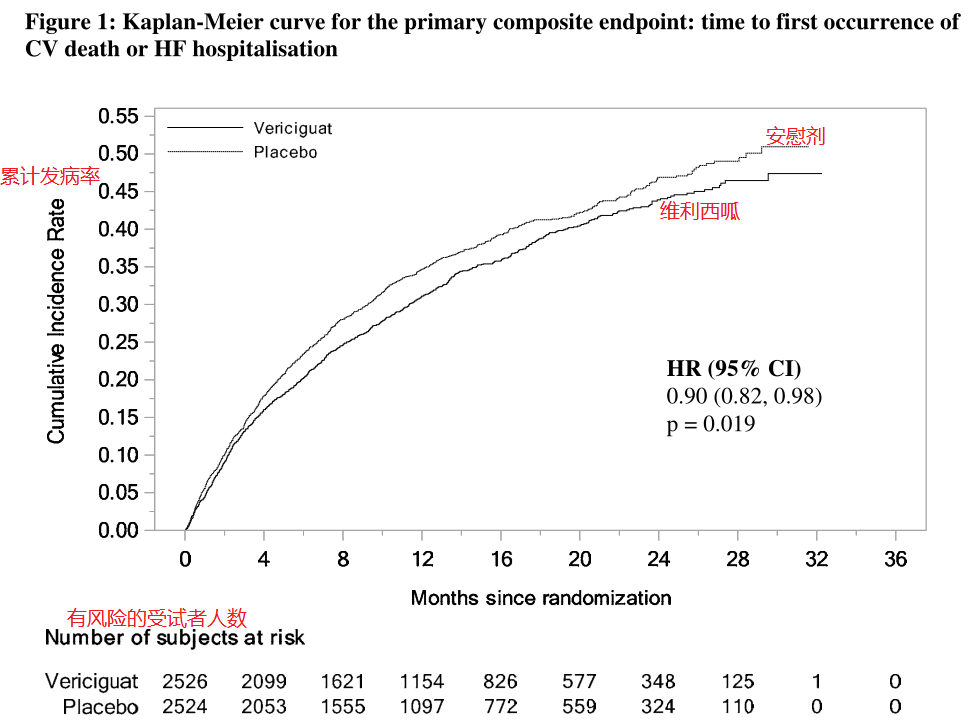
图为欧洲药监局维利西呱说明书中治疗心衰疗效数据根据卡普兰-梅尔计算模型,累计发病率介于0-1之间,从下图可以明显看出维利西呱组所有时期的累计发病率都小于安慰剂组,32周后,因患者发病、失联或未知原因,发病率趋向于平缓。
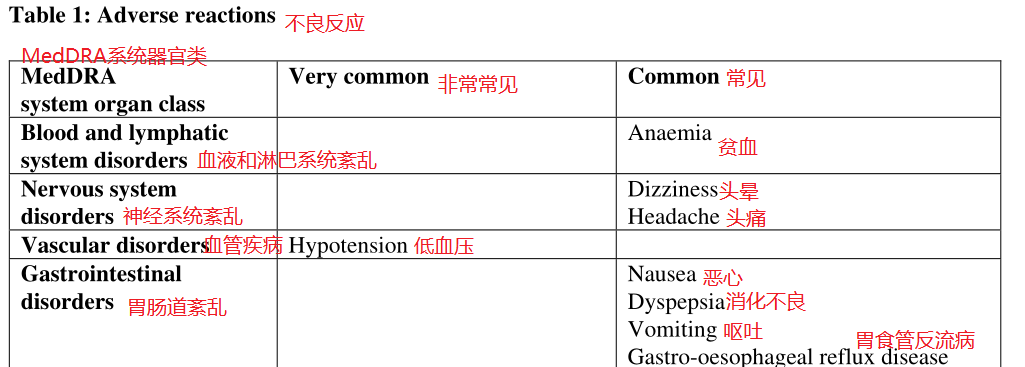
维利西呱的安全性在一项III期研究中进行了评估,该研究共包括2519名接受维利西呱治疗的患者(每日最多10mg),从临床研究中得到的维利西呱的不良反应按MedDRA系统器官类别和频率列于下表。频率被定义为非常常见(≥10%)、常见(1%~10%)。
最常见的不良反应:低血压(16.4%)。
常见的不良反应:贫血、头晕、头痛、恶心、消化不良、呕吐、胃食管反流病。
注意:过量服用维利西呱可能会导致低血压。如有必要,提供对症治疗。由于本品与蛋白质结合率高,因此不太可能通过血液透析去除。
 维利西呱
维利西呱 片剂
2.5mg*28|5mg*98|10mg*98
 德国拜耳
德国拜耳
进一步降低心血管死亡和因心衰住院风险
2025-05-15 16:55:04
2025-05-15 16:51:06
2025-05-15 16:41:43
2025-05-15 16:37:30
2025-05-15 16:25:47
2022-09-01 16:41:48
2022-09-01 17:47:05
2022-07-11 17:10:49
2022-05-12 17:51:01
2022-05-24 16:17:48