长春瑞滨主要作用于肿瘤细胞的DNA合成后期,通过阻止微管蛋白聚合形成微管,并诱导微管解聚,使肿瘤细胞的有丝分裂增殖停止于有丝分裂的中期,达到抗肿瘤的目的。
药品称呼
通用名:长春瑞滨
商品名:盖诺
全部名称:长春瑞滨,长春瑞宾,盖诺,酒石酸长春瑞滨,vinorelbine,Vinorelbine Tartrate Injection
禁忌
妊娠期、哺乳期妇女及严重肝功能不全者禁用。
贮藏
避光冰箱(4℃)内保存
作用机制
本品为长春碱半合成衍生物,主要通过抑制微管蛋白的聚合,使细胞分裂停止于有丝分裂中期,是一细胞周期特异性的药物。
主要作用是与微管蛋白结合,因之使细胞在有丝分裂过程中微管形成障碍。NVB为周期特异药物,作用近似VCR,浓度>12nmol时可阻断G2--M期,除了对有丝分裂的微管以外,对轴突微管也有亲和力,因之可引起神经毒性,但较VCR要轻。
进入血内后大部(80%)与蛋白结合,96小时后降到50%。通过放射性核素标记的药物说明在72小时内尿中排出不足12%,在人和猿中50%~70%由粪中排出(3~4周)。所以肾功能异常的患者可用此药,但因主要由胆道排出,所以胆管阻塞的人应减量。
安全与疗效
为研究长春瑞滨(NVB)联合顺铂(DDP)方案(NP方案)治疗吡柔比星(THP)方案耐药的晚期非小细胞肺癌(NSCLC)复发、转移的近期疗效和毒副反应。采用NP方案对曾用THP方案治疗大于2周期后进展或复发、转移的晚期非小细胞肺癌41例进行治疗,21天为1周期,完成2周期后评价疗效。
结果:部分缓解(PR)17例,稳定(SD)15例,进展(PD)9例。总有效率41.5%。WHO标准Ⅲ,Ⅳ度白细胞下降占87.9%,主要为血液毒性。
结论:长春瑞滨联合顺铂治疗吡柔比星耐药的晚期非小细胞肺癌仍是可供选择的有效方察,疗效确切、毒副反应可耐受。
完整说明书详见:
适应症
适用于不可手术切除的局部晚期或转移性非小细胞肺癌,和转移性乳腺癌的单一用药和联合化疗。
用法用量
1.推荐剂量:
作为单一用药时,前三次给药推荐剂量为 60mg/m²,每周服用1次,3周为一个疗程。后续治疗推荐剂量为80mg/m²,每周服用1次。
2.剂量调整:
(1)三次用药后推荐剂量为80mg/m²,但前三次应60mg/m²剂量时,嗜中性粒细胞若曾有一次低于 500/mm³或超过一次低至 500~1000/mm³ 间的患者应仍维持60mg/m²剂量。
(2)在使用80mg/m²的剂量期间,若嗜中性粒细胞数量出现低500/mm³的情况或者超过一次在 500~1000/mm³之间,需等到嗜中性粒细胞数量恢复正常才能继续用药,并且将剂量由 80mg/m²/周减少至60mg/m²/周。
不良反应
常见不良反应包括骨髓抑制、贫血、血小板减少、恶心、呕吐、腹泻和便秘、感染、食欲不振、失眠、腱反射消失、头痛、血压不稳定、呼吸困难、脱发、肌痛、排尿困难、乏力、体重下降等。
禁忌
1.已知对长春瑞滨、或其他长春花生物碱类、或本品中的任何成分过敏。
2.患有明显影响本品吸收的疾病。
3.既往有胃部或小肠切除的重大手术史。
4.血小板计数<100000mm³。
5.长期氧疗患者。
6.嗜中性粒细胞计数<1500mm³,或目前或最近(2周内)发生严重感染。
贮存方法
遮光,密闭,在冷处(2-8℃)保存。
适用人群
成人
药物相互作用
1.禁止与黄热病疫苗联合应用,会发生致命的全身性疾病。
2.不建议与减活疫苗与苯妥英类药物共同使用,一般建议使用灭活疫苗。
3.谨慎与环孢素、他克莫司、依维莫司、西罗莫司等药物共同使用,过度免疫会导致淋巴组织增生。
4.与伊曲康唑、泊沙康唑、酮康唑等药物共同使用时,可能会增加长春花生物碱的神经毒性。
5.不建议与CYP3A4强诱导剂或抑制剂共同使用。
有效期
36个月
剂型
胶囊剂
生产厂家
法国Pierre Fabre
成分
本品主要成分是酒石酸长春瑞滨,化学结构式为:
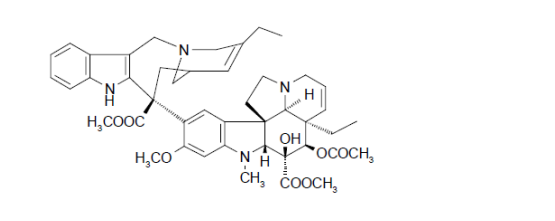
性状
本品为浅棕色软胶囊,内容物为粘性、澄清的浅黄至橘黄色溶液,基本无可见颗粒。
注意事项
1.本品应直接吞服,若不慎咀嚼或吮吸本胶囊,应用水或生理盐水漱口。
2.若不慎接触胶囊内液体,应用水或生理盐水进行彻底冲洗。
3.已损坏胶囊请勿吞服,请返还医师,以便进行适当销毁。
4.服药后出现呕吐反应,不需再次服用所需剂量,可以给予止吐药物进行治疗。
5.不推荐与减毒的活性疫苗同时使用。
(以上内容参考自中文说明书2020.12版)



 法国Pierre Fabre
法国Pierre Fabre  在线咨询
在线咨询 
 德国Riemser Pharma GmbH
德国Riemser Pharma GmbH
 美国礼来Lilly
美国礼来Lilly
 美国邓德利安Dendreon
美国邓德利安Dendreon
 孟加拉伊思达
孟加拉伊思达 用法用量
用法用量